GFME bulletin n°42
Suite

Glioblastome Association Michèle Esnault (GFME) Bât A, boîte 4, 22 bd Camille Flammarion 13001 Marseille
Recevoir gratuitement par courrier le bulletin à domicile
Télécharger le bulletin en .pdf

Professeur David A. Reardon Dana Farber Cancer Institute, Harvard
Le mot du président
J’ai mis en photo de ce numéro le docteur David A. Reardon, neuro-oncologue dans le grand centre américain Dana Farber Cancer Institute, DFCI, à Harvard, ville de l’agglomération de Boston dans le Massachussetts, au Nord-est de New York. David A. Reardon est aussi Professeur à l’école de Médecine de Harvard, Harvard où ont étudié Barak Obama, Bill Gates et Marck Zukerberg.
Une biopsie qui tourne mal
Dans un grand hôpital des Hauts de France, un papa de 2 jeunes enfants, 1 an et 4 ans, est hospitalisé le 27 juin 2016, suspicion de glioblastome. Le 8 juillet on pratique une biopsie avec anesthésie générale. L’intervention se passe mal, hémorragie probablement et coma. Le papa décèdera le lendemain en réanimation laissant une veuve et 2 jeunes orphelins éplorés.
L’immunothérapie en marche
Après les traitements classiques qui tuaient les cellules saines comme les cellules tumorales, après les traitements ciblés qui agissaient sur le génome des tumeurs, l’immunothérapie, quelque chose d’ancien, vient d’être redécouverte, et fait actuellement un grand bond en avant après son 1er succès sur le mélanome. Faire reconnaître, par le système immunitaire, une cellule tumorale comme étrangère, du non-soi, tel est le formidable défi des nouveaux traitements et l’ambition des 400 essais d’immunothérapie qui ont lieu actuellement dans le Monde sur le glioblastome.
Un système immunitaire complexe.
L’immunothérapie consiste à utiliser les défenses naturelles de l’organisme contre les cancers. Notre système immunitaire est complexe car s’il reconnait les cellules étrangères, le non soi, les virus et bactéries, il ne reconnait pas nos propre cellules, notre soi, même cancéreux. C’est une puissante armée de 22 cellules, macrophages, neutrophyles, natural killer, complément, monocytes, cellules dendritiques, lymphocytes T, T helper, T mémoire, et chacune de ces cellules a jusqu’à 5 fonctions différentes. S’ajoutent des protéines qui circulent dans le sang, les immunoglobulines ou anticorps, il en existe plusieurs milliards en 5 types dans le corps humain qui luttent rapidement et se sacrifient pour notre survie face à nos ennemis au développement rapide, virus, bactéries qui doublent toutes les 20 minutes. Le 1er à entrer en action est le macrophage (gros mangeur) qui avale l’antigène. Il est attiré par des signaux inflammatoires, histamine des basophiles, cytokines des macrophages déjà présents ou des substances libérées par des cellules en difficulté (nécrose, apoptose). Les macrophages reconnaissent les antigènes par les PAMPs (Pathogen Associated Molecular Patterns), molécules que l'on retrouve chez de nombreux pathogènes. Si le macrophage repère un PAMP, il passe à l'attaque et ingurgite l’antigène (immunité innée). Il va ensuite présenter les morceaux de l’antigène dévoré aux lymphocytes T CD4+, l’immunothérapie commence.
L’interview du docteur Reardon, Dana-Farber, Harvard, en résumé
Une thérapie qui donne un avantage important de survie n’existe pas pour le glioblastome. L'immunothérapie peut offrir une réponse. Nous avons des traitements qui peuvent aider nos malades, mais le problème est la durabilité de l'avantage, car tôt ou tard la tumeur acquiert la capacité d'éviter les effets du traitement et le glioblastome devient vite résistant. Un avantage solide a été observé avec le blocage PD1-PDL1 dans le mélanome métastasique, le cancer du poumon, et dans le carcinome rénal. Je pense que c'est un aspect passionnant que ces thérapies et nous espérons qu'elles réussiront pour les tumeurs de cerveau. Plusieurs essais d'immunothérapie présentés à l'ASCO 2016 ont montré des données préliminaires prometteuses. Les données d'efficacité de ces essais n'avaient pas encore assez de délai, mais il y avait quelques données intéressantes de sécurité qui ont été présentées avec le nivolumab (Opdivo), puis le MEDI4736, et le pembrolizumab (Keytruda). Quelques données préliminaires d'efficacité ont aussi été enregistrées. Nous devrions avoir des données pour la fin de l'année 2016, ou au 1er trimestre 2017. Nous sommes très enthousiasmes au sujet de ces 2 inhibiteurs de contrôle, PD-1 et PD-L1. Il y a aussi des données précliniques croissantes qui utilisent des modèles animaux de xénogreffes de glioblastomes intracrâniennes sur des animaux immunocompétents et qui montrent que ces 3 agents peuvent avoir un avantage considérable pour les animaux avec glioblastome. C'est toujours passionnant de voir de tels résultats précliniques qui montrent une promesse d'efficacité et de pouvoir les valider sur des malades. Dans les modèles précliniques, il y a des données passionnantes pour supporter des essais cliniques. Pour le glioblastome, l'infiltrat immunitaire est classé dans le milieu du spectre des cancers. Un plus haut degré d'infiltrat est connu sous le nom de microenvironnement de tumeur chaud, et un degré moindre microenvironnement de tumeur froid. Le glioblastome est dans le milieu, mais probablement plus vers le spectre froid que chaud. Un autre facteur important est le fardeau mutationnel associé avec les cancers qui peut être différent mais qui peut surtout prédire l’immunogénicité de la tumeur. Le glioblastome se situe encore vers le milieu du spectre des cancers quant au fardeau mutationnel moyen. Il n'est pas tout à fait à la fin basse, mais pas aussi haut que mélanome ou le cancer du poumon qui répondent bien à ces inhibiteurs PD1-PDL1. La plupart des données place le glioblastome dans la gamme centrale pour l'immunogénicité. Nous savons aussi que de nombreux traitements standards que nous utilisons, en particulier la radiothérapie, peuvent rehausser considérablement l'inflammation (immunogénicité) dans le microenvironnement de la tumeur. Quand nous parlons d'activité immunitaire dans les tumeurs, nous devons savoir que c'est un processus très dynamique, car l'activité immunitaire varie avec le temps. Une tumeur qui est opérée et analysée à la sortie de la salle d'opération peut être très différente de la même tumeur après que le malade eut suivi la radiothérapie surtout au niveau des cytokines initiales qui conduisent, stimulent ou inhibent les réponses immunitaires. L'infiltrat immunitaire peut changer aussi très considérablement au cours de la maladie et être associé avec des interventions différentes. Nous avons besoin de réfléchir à ce que c'est une mesure très dynamique qui peut changer selon une variété de facteurs et d’influences. Il y a un travail passionnant et progressif avec les stratégies de vaccins et cela depuis 15 ans que nous y avons travaillé, et que nous essayons de produire des vaccins pour les malades avec des tumeurs de cerveau. De nombreux centres sont aussi actuellement impliqués. Je pense que beaucoup d'optimisations se sont produites en apprenant des premiers essais qui ont été réalisés. Une meilleure approche de vaccin est aussi l'identification de néoantigènes (antigènes de la tumeur) spécifiques à la tumeur. Ce sont les mutations présentes dans une tumeur donnée qui engendre des protéines qui vont seulement être présentes dans les cellules de la tumeur et pas dans les cellules normales. Nous savons par la recherche que le codage de ces mutations associé avec les peptides qui ont subi une mutation peuvent être très immunogéniques et nous essayons d'utiliser le codage de ces mutations pour prendre l'avantage avec cette technologie qui est actuellement disponible par analyse génomique haut débit. L'identification du codage des mutations et des algorithmes peuvent aider à prédire lequel des néoantigènes est très probablement immunogénique pour les malades. L'avantage de toute cette dernière technologie est maintenant une réalité, et sa traduction en un vaccin basé sur le néoantigène du patient est une application très passionnante pour l'approche du vaccin chez les malades avec des tumeurs de cerveau. Il y a aussi plusieurs essais de vaccin qui sont maintenant en phase III avancée et je pense que les résultats de ces essais devraient être rapportés dans la prochaine année 2017. Nous sommes pleins d'espoir et nous devrions voir quelques résultats prometteurs de ces essais qui touchent à leur fin. Je pense aussi que la chose la plus prometteuse va exiger des traitements de combinaison où nous pourrons utiliser une stratégie pour rehausser l'immunogénicité en combinaison avec une stratégie thérapeutique visant à diminuer l'immunosuppression associé à la tumeur. Cela va nous permettre d'accélérer les réponses immunitaires anti-tumorales, et en même temps de diminuer les facteurs immunosuppressifs dans les tumeurs, avec une tendance à les déployer rapidement pour les protéger des réponses anti-tumorales spontanées d’échappement aux traitements. Nous aurons besoin d'une combinaison de stratégies pour faire les deux choses à la fois. Nous devrons trouver l’approche la plus prospère pour optimiser l'avantage de ces nouveaux médicaments pour nos malades.
La chirurgie des gliomes de grades II à IV améliore les symptômes.
Actualité 564 du 11/07/2016
C’est une équipe américaine de l’Oklahoma qui s’est intéressée aux symptômes de la maladie réglés avec la chirurgie. C’est une analyse rétrospective sur 56 malades ayant été opérés dans leur centre pour un gliome grade II à IV. Tous les malades ont été vus 2-4 mois après la chirurgie, et ont apprécié la persistance ou non des symptômes par rapport à ceux existants avant la chirurgie. Parmi ces symptômes avant chirurgie, le mal de tête a été résolu chez 18/27 après chirurgie, la faiblesse résolue chez 8/14, le statut mental amélioré chez 8/12, les problèmes de vision chez 7/11, la nausée chez 5/7, et l'ataxie chez 4/5. Le mal de tête a été mieux résolu chez les malades avec des tumeurs frontales ou temporales. L'indice de karnofsky (KPS) de 70 ou moins a été associé avec un plus long séjour à l'hôpital, en postchirurgie. Les plus Jeunes malades ont éprouvé une meilleure résolution de leur statut mental. Cette analyse fournit des taux d’amélioration des symptômes des patients après la chirurgie des gliomes de grade II-IV, dans les mois qui suivent la chirurgie et peuvent être portés à la connaissance des malades.
Pubmed 27588717
L’injection intracrânienne de resveratrol inhibe la croissance et l'infiltration du glioblastome et celle des cellules souches
Actualité n° 566 du 11/07/2016
Encore une nouvelle étude sur le resveratrol américano-syngapourienne cette fois. Ils ont étudié les effets du resveratrol sur la prolifération cellulaire, la capacité à la formation des sphères, et l'invasion en utilisant des cellules de glioblastome dérivées de malades multiples contenant des cellules souches (GSC) ainsi que des cellules de glioblastome U87 pour analyser les changements oncogéniques d'AKT dans la tumeur ainsi que la régression de p53. Le resveratrol a aussi été testé in vivo contre les cellules de gliomes U87 implantées en xénogreffes sur le flanc de souris en utilisant des méthodes de livraison multiples, y compris l'injection directe dans la tumeur par CED. Finalement, le resveratrol a été délivré directement dans la tumeur pour frapper fort le tissu tumoral et déterminer la toxicité à des concentrations supportables par le parenchyme de cerveau normal. Le resveratrol a inhibé considérablement la prolifération du gliome U87 et des cellules souches GSC dérivées de multiples malades, en démontrant des concentrations inhibitrices semblables à travers ces lignées aux phénotypes hétérogènes. Le resveratrol a aussi inhibé la capacité à la formation de sphères ce qui suggère des effets sur les cellules souches. Dans les cellules U87 de gliome et les cellules souches GSCs, le resveratrol a réduit la phosphorylation d'AKT et l'expression de p53. L'administration du resveratrol par gavage oral ou liquide des xénogreffes de glioblastome a conduit à une croissance considérablement étouffée. L'injection intratumorale (CED) de resveratrol a conduit à la réduction des tumeurs. L'injection intracrânienne de resveratrol conduit à des concentrations locales 100 fois supérieures à livraison intraveineuse, et cela sans toxicité apparente. En conclusion, le resveratrol a bien inhibé la croissance du glioblastome et des cellules souches ainsi que l'infiltration, en agissant partiellement par désactivation d'AKT et par p53. La capacité du resveratrol à moduler AKT et p53, aussi bien que de nombreuses autres voies antitumorigéniques, est une découverte attrayante pour une thérapie contre une tumeur génétiquement hétérogène telle que le glioblastome. La livraison convection-rehaussée (CED) pourrait être utilisée pour accomplir et maintenir des doses thérapeutiques dans le cerveau. La nature non-toxique du resveratrol et ses effets sur le glioblastome en font un candidat irrésistible pour augmenter les thérapies courantes contre le glioblastome.
Pubmed : 27419830
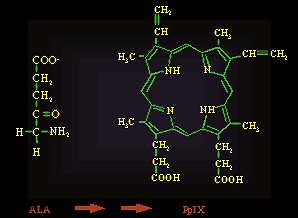
Les glioblastomes humains accumulent de la protoporphyrine IX quand ils sont soumis au 5-acide aminolévulinique hydrochloride ( 5-ALA, Gliolan) qui les rendent sensibles à un traitement photodynamique au laser.
Thérapie photodynamique
Le 5-ALA, produit allemand, n’a jamais eu la confiance des neuro-chirurgiens ni des organismes de santé, utilisation complexe, effets secondaires, contraintes d’injection. Voila une découverte qui pourrait changer la donne. C’est un produit dérivé de la chlorophylle (du grec Khloros vert et phullon, feuille), le colorant des feuilles mais aussi du chewing gum qui absorbe la lumière et la convertit en énergie organique. Elle améliorerait notre hémoglobine. Le 5 ALA est actuellement utilisé pour la fluorescence des cellules de tumeur. Après application du 5-ALA, il y a production de protoporphyrine IX, un radiosensibilisateur qui génère des oxygènes singulets, oxygène instable quand il est exposé avec la lumière visible 400–640 nm. L’oxygène singulet, noté 1O2 est un état instable de l'oxygène, car excité, de la molécule d’oxygène qui se forme si on mélange de l'eau oxygénée H2O2 à de l’eau de Javel NACIO par action des ions hypochlorite ClO- sur le péroxyde H2O2, réaction qui s'accompagne d'une très faible luminescence rouge foncé par relaxation des molécules d'oxygène singulet 1O2. Les glioblastomes humains accumulent de la protoporphyrine IX quand ils sont soumis au 5-ALA. Les glioblastomes contiennent un petit nombre de cellules souches (GSC) capables de produire de nouvelles tumeurs, cellules particulièrement résistantes aux thérapies et suspectées d'être les responsables des récidives. Le 5-ALA peut servir de médiateur dans une approche de thérapie photodynamique consistant à utiliser l'accumulation du photosensibilisateur, la protoporphyrine IX (PPIX) dans les cellules de glioblastome GBM après application de 5 ALA. Quand on expose ensuite les cellules au laser à la longueur d'onde de 635nm la PPIX commence une réaction photochimique qui résulte en la génération d'oxygène réactive qui tue les cellules de la tumeur. Le fait que les cellules souches GSC accumulent la PPIX et deviennent sensibles à la thérapie photodynamique 5-ALA/PDT était inconnu à ce jour. On observe bien chez les cellules souches GSC humaines dérivées des tumeurs fondamentales et soumises au 5-ALA une accumulation temps-dépendante de PPIX. L'exposition à la lumière d’un laser de 635nm a bien tué ensuite les cellules souches GSC et de façon notable, alors que le traitement avec 5 ALA sans attente de la production de PPIX n'a aucun effet sur les cellules souches lorsqu’on les expose au laser. En résumé, c’est la 1ère fois que l’on constate que les glioblastomes peuvent accumuler de la protoporphyrine IX après exposition au 5-ALA et devenir sensibles à la thérapie photodynamique par laser. On devrait en reparler.
Pubmed n° 27588717
Avances et défis, les stratégies de vaccinations cellulaires dendritiques pour glioblastome.
Actualité n° 569 du 10/08/2016
C’est une étude de la grande équipe américaine de Duke qui nous fait part des avancées dans ces vaccins dendritiques DC qui n’ont jamais bien réussi ces 20 dernières années. Des avancées récentes d’immunothérapie par vaccination cellulaire dendritique montre des résultats encourageants et prometteurs dans les essais cliniques pour améliorer la survie patiente. Dans cette optique, ils proposent à Duke, des approches différentes pour amorcer, instruire les cellules dendritiques afin d’obtenir l'efficacité anti-tumorale maximale contre le glioblastome. Leurs conclusions ont été récemment complétées par des essais cliniques actuellement en cours sur le glioblastome. De nouvelles méthodes comme 'fastDCs' et des vaccins ciblés DCs in-vivo peuvent offrir un traitement plus efficace comparé aux vaccins DC traditionnels. C’est un formidable défi à résoudre que de contrer le dysfonctionnement des cellules T provoqué par l'immunosuppression du glioblastome.
Pubmed : 27500911
Les derniers essais cliniques en cours d’après le site Clinicaltrials
1-(06/2016), Phase II, Etats-Unis, plusieurs centres dont Cleveland, Tesevatinib pour glioblastome récurrent.
Le Tesevatinib est un inhibiteur EGFR, un de plus, mais aucun n’a jamais marché.
Original
2- (07/2016), Phase II, Etats-Unis mais aucun hôpital désigné, CED (Convection orientée) de MDNA55 pour glioblastome récurrent.
MDNA55 est un inhibiteur des récepteurs à interleukine IL-4. La CED est peu utilisée en thérapie.
Original
3-(06/2016), Phase I/II, Chine, Percellvac2 pour glioblastome récurrent.
Comme il s’agit d’un des 1ers essais cliniques chinois, on ne sait absolument rien encore de ce vaccin personnalisé. On sait qu’il est personnalisé, et donc probablement un nième vaccin dendritique.
Original
4-(07/2016), Phase I, Etats-Unis, Duke, Injection de 4 Vaccins PEP-CMV, cytomégalovirus, avec tétanos-diphtérie modifiés lors des cycles adjuvants de temozolomide.
On se demande toujours pourquoi ce grand centre s’intéresse aux cytomégalovirus car des virus ce n’est pas ce qui manque dans le cerveau et à ce jour aucun n’a réussi à détruire une cellule tumorale.
Original
5-(07/2016), Etude pilote préclinique de phase I, Chine, vaccin autologue anti EGFRvIII CAR T, + cyclophosphamide + fludarabine pour glioblastome récurrent.
Dans cet essai chinois, on copie ce qui se fait dans d’autres cancers.
Original
6- (06-2016), phase II, Suède, ALECSAT + Stupp pour glioblastome nouvellement diagnostiqué.
Alecsat est un vaccin autologue avec des cellules lymphoïdes effectrices spécifiques. 3 injections toutes les 4 semaines et 1 ensuite tous les 3 mois.
Original
7-(04/2016), phase non précisée, Allemagne, détermination du phénotype immunitaire et corrélation avec le résultat.
On examine à la chirurgie, IDH1 muté ou IDH1 wild type, EGFR, MGMT, Karnofski puis par prise de sang le phénotype immunitaire.
Original
8-(07/2016), phase pilote préclinique Etats-Unis, Dana-Farber, déterminateur précoce des paramètres pharmacodynamiques immunologiques de PD1 pour un traitement avec Pembrolizumab de patients réopérables à la récidive.
Vu le prix du produit, une étude sur les répondeurs possibles est une bonne chose.
Original
9-(01/2016), phase II, Etats-Unis, essai d’immunothérapie avec Tremelimumab et/ou Durvalumab (MEDI 4736) pour glioblastome récurrent.
Tremelimumab et Durvalumab sont des inhibiteurs PD1-PDL1. Medi est déjà en essai seul avec des résultats encourageants. On veut voir la synergie avec le tremelimumab.
Original
10-(08/2016), phase pilote, préclinique de Cabozantinib pour gliome pédiatrique de haut grade récurrent.
Le cabozantinib est un inhibiteur à cibles multiples, HGFR, c-Met, VEGFR utilisé dans le cancer de la thyroïde et du rein. On l’essai chez les enfants.
Original
Et ceci n’est qu’une petite liste des essais du dernier trimestre.
Ils nous ont quittés
-Le 08/07/2016, Rémi, 31 ans, le mari de Noémie, le papa de Léa, 4 ans et de Zoé, 1 an.
-Le 10/07/2016, Virginia, 47 ans, la fille de Christian
-Le 20/07/2016, Michel, 61 ans, le frère de Nicole
-Le 12/08/2016, Marlène, 71 ans, la maman d’Alice
-Le 13/09/2016, Pierre, 75 ans, le conjoint d’Eliane
-Le 17/09/2016, Jean-Paul, 78 ans, le papa de Laure, Marie et Pauline.
A toutes les familles, GFME adresse ses plus sincères condoléances.
Les dernières publications postées sur Internet
579-Les glioblastomes frontaux sont biologiquement distincts des non frontaux (08/09/2016)
578-Le traitement avec la décitabine des cellules souches de gliomes GICs accroît la reconnaissance immunitaire et la mort cellulaire des gliomes***
(08/09/2016)
577-La radiochimiothérapie avec temozolomide concomitant contre-indiqué pour les jeunes adultes <=50 ans diagnostiqués avec gliome anaplasique.
(06/09/2016)
576-Impact pronostique de la classification OMS 2016 des gliomes diffus dans la cohorte POLA française (31/08/2016)
575-Changements dans les expressions de PlGF et MET-HGF entre les glioblastomes initiaux et récurrents
(31/08/2016)
574-La Berberine induit l'autophagie dans le glioblastome en ciblant la voie AMPK/mTOR/ULK1 (28/08/2016)
573-Les applications émergentes des ultrasons thérapeutiques en neuro-oncologie, ablation de la Tumeur et bien plus (25/08/2016)
572-Les cellules souches de gliomes migrantes conservent les marqueurs cellulaires souches et engendrent de nouvelles tumeurs sur des xénogreffes. (16/08/2016)
571-Les vaccins tumeurs-dérivés qui contiennent CD200 inhibent l'activation immunitaire, des implications pour l'efficacité de l'immunothérapie
(11/08/2016)
570-Ce qui est nouveau dans le traitement du glioblastome, les thérapies ciblées ou l'immunothérapie ?
(10/08/2016)
La fréquentation du site n’est jamais descendue cette année en dessous de 1000 visites/jour.
Si on compare les 8 premiers mois de l’année 2016 à ceux de 2015, ce sont 299.111 visites en 2016 contre 237.562 en 2915, en augmentation de 25,9 %.
******************************
Rendez-vous pour le prochain numéro, le n° 43 en Janvier 2017
Glioblastome Association
Michèle Esnault (GFME)
Bât A, boîte 4
22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 €/Renouvellement 7,5 €.
Reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N

Rendez-vous pour le prochain numéro, le n° 43 en Janvier 2017
Glioblastome Association
Michèle Esnault (GFME)
Bât A, boîte 4
22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 €/Renouvellement 7,5 €.
Reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N
Michèle Esnault Fondatrice de GFME en 2001 (15 ans)