GFME, journal n° 15
Suite

Glioblastome Association Michèle Esnault (GFME) Bât A, boîte 4, 22 bd Camille Flammarion 13001 Marseille
Recevoir gratuitement par courrier le bulletin à domicile
*****Télécharger le bulletin en .pdf*****

Nino, 6 ans, qui a succombé, que la vie est parfois injuste
-Le 18/03/2009, Nino, 6 ans, le fils de Christophe et Elodie nous quittait des suites d'un gliome du tronc cérébral
Le mot du président
Depuis un an, une nouvelle thérapie a considérablement allongé la survie des patients avec glioblastome, une combinaison de chimiothérapie antitopoïsomérase et un médicament intelligent Avastin (Bevacizumab), anticorps monoclonal qui bloque le développement des nouveaux vaisseaux sanguins pour l’approvisionnement de la tumeur. Ce traitement a été validé le 5 mai 2009 en 2ème ligne en cas de récidive ou progression sous Temodal, le traitement standard de 1ère ligne. Mais les résultats sont encore inconstants et la tumeur arrive à contourner l’obstacle en fabricant elle-même ses propres vaisseaux sanguins par les cellules souches tumorales pluripotentes. Cet échappement fait l’objet de toute les études actuellement et de nouveaux traitements devraient voir le jour dans les prochains mois. Le recherche avance, les survies s’améliorent et la guérison viendra si toutes les forces, tous les savoirs, tous les soignants, tous les chercheurs s’unissent pour ce grand challenge.
Va-t-on vers Avastin dès le début, et Temodal 7/28 à 150mg/m2 ?
L’Asco va présenter fin mai un essai clinique comparant les résultats de deux groupes, le groupe 1 recevant Avastin dès le départ tous les 15 jours à 10 mg/kg et la radiochimiothérapie avec Temodal journalier à 75 mg/m2 suivi de 6 cycles de Temodal à 150 mg/m2 , 7/28 jours, et un groupe 2 recevant le même régime sans Avastin. Les résultats de survie vont du simple au double. PFS à 6 mois du groupe 1 de 77,5% et du groupe 2 de 51,6%. PFS médian du groupe 1 de 17 mois contre 7 mois au groupe 2. L'OS médian n’est pas encore atteint dans le groupe 1 et est de 17 mois dans le groupe 2. OS à 1 et 2 ans de 83% et 57% dans le groupe 1 et de 72% et 6,5% dans le groupe 2.
Avastin, 10mg/kg tous les 15 jours dès le départ et Temodal , 7/28 jours à 150 mg/m2 après la radiochimiothérapie devraient voir le jour.
L'essai n° 2017
Promesses de survies à long terme (18,5% à 4 ans) pour La radio chimiothérapie avec CCNU et Temodal sur glioblastome nouvellement diagnostiqué
Une équipe allemande vient de publier des résultats excellents d’un essai clinique sur la combinaison de deux alkylants oraux, somme toute assez voisins, CCNU et Temodal en complément de la radiothérapie. 2 groupes, le premier de 31 patients avec glioblastome a reçu 100 mg/m2 de CCNU le jour 1 et 100 mg/m2 de Temodal, les jours 2-6 pendant la radiothérapie de 60 grays en 6 semaines et après sur 6 cycles. Un second groupe a reçu un dosage plus intense de 110 mg/m2 de CCNU et 150 mg/m2 de Temodal. Dans la cohorte entière, la survie totale médiane (mos) était de 23,1 mois. 47,4% ont survécu à 2 ans et 18,5% ont survécu à 4 ans. Après un suivi médian de 41,5 mois, la mos n'avait pas été atteinte dans le groupe plus intense. Les survies étaient considérablement plus élevées dans le groupe intense que dans le groupe standard de 22,6 mois. Dans le groupe intense, 4/8 malades ont survécu pour au moins 56 mois, dont 2/8 sans le retour de la tumeur. Il y avait des différences considérables selon la méthylation du promoteur du gène MGMT dans le tissu de la tumeur qui a été associé avec une survie considérablement plus longue de 34,3 mois pour le groupe méthylé, contre 12,5 mois dans le groupe non méthylé.
Pubmed : 19188676 et GFME : 273
Une simple prise de sang, demain pour prédire le potentiel angiogénique des tumeurs
Fini, le casse tête des neuro-oncologues pour examiner le caractère angiogénique d’une tumeur, IRM avec ou sans contraste, Pet Scan. Une équipe américaine de l’Hôpital Presbytérien de New York vient de découvrir qu’une simple prise de sang suffisait. La néo vascularisation des tumeurs de cerveau malignes est un phénomène peu compris et aucun essai quantitatif non-invasif pour corréler la vascularisation du gliome et son caractère agressif clinique associé n'a jamais été effectué. Les précurseurs des cellules endothéliales circulants sont des précurseurs vasculaires recrutés depuis la moelle osseuse à travers la circulation pour former les nouveaux vaisseaux sanguins de la tumeur. Ces cellules ont été mesurées chez les malades qui ont subi la chirurgie pour glioblastome. 55 malades avec gliomes de plusieurs grades ont eu des prises de sang au moment de la chirurgie et lors des visites ultérieures. Le sang a été séparé entre plasma et fractions cellulaires. Le plasma a été utilisé avec des cellules endothéliales de veine ombilicale humaine. La fraction contenant les précurseurs des cellules endothéliales a été analysée par cytométrie, ce qui a permis de les séparer et de les compter. Les échantillons pathologiques ont été examinés d'abord au temps de la chirurgie puis pendant les visites ultérieures. Le plasma dérivé du sang des malades avec glioblastome donnait des points considérablement plus hauts sur l'échelle angiogénique que celui des malades avec gliomes de bas grade. Tous les malades avec glioblastome avaient également des nombres plus élevés de précurseurs de cellules endothéliales issus de la moelle osseuse exprimant CD 133 et le récepteur du facteur de croissance endothélial VEGFR 2 dans leur sang qu'au temps de la chirurgie. Les cellules exprimant CD 133 ont varié de moins de 0,1% à 1,6% de la population des globules blancs mononucléaires, ou approximativement 200.000 cellules chez quelques malades. Une corrélation importante a été observée entre le pourcentage de précurseurs des cellules endothéliales dans le sang au temps de la chirurgie du glioblastome et la survie. Ces résultats suggèrent que le plasma et les précurseurs des cellules endothéliales CD133+ et VEGFR2+ présents dans le sang des malades avec gliome peuvent être utilisés comme bio marqueur de remplacement pour mesurer l'angiogénicité tumorale. Ces résultats peuvent être utilisés pour prédire le caractère agressif de la tumeur.
Pubmed : 19404145 et GFME : 272
La FDA américaine valide en accéléré Avastin pour le glioblastome en récidive ou progression après la thérapie antérieure
San Francisco, le 5 mai 2009
L'efficacité d'Avastin sur le glioblastome n’est plus à démontrer. C’est sans attendre des résultats d’essais de phase III randomisés que la FDA vient de valider en accéléré Avastin pour le traitement du glioblastome en 2ème ligne, en échec de Temodal. Un essai de phase III pour les malades récemment diagnostiqués avec glioblastome démarrera sous peu. L'approbation accélérée est une approbation provisoire. La FDA s’est basée sur un avis d’experts et les résultats de 2 essais cliniques de phase II, l’un, AVF3708G, multicentrique, de 167 malades avec glioblastome randomisés en 2 bras, 85 malades sur Avastin seul et 82 sur Campto-Avastin et l’autre NCI 06-C-0064E de 56 malades avec Avastin seul. Dans le 1er essai, 26% des 85 malades traités avec Avastin seul avait une réponse totale ou partielle, et la durée médiane de la réponse chez ces malades était de 4,2 mois (3,0 mois, 5,7 mois). L'âge médian des malades traités du groupe Avastin seul était de 54 ans, 32% de femmes, 81% en première rechute, 45% avec un indice de Karnofsky (KPS) de 90 à 100 et 55% de 70 à 80. Dans l’autre essai NCI 06-C-0064E à bras unique de 56 malades avec Avastin seul, le taux de réponse objectif (totale ou partielle) était de 20% avec une durée médiane de réponse de 3,9 mois (2,4 mois-17,4 mois). Pour les 167 malades des deux bras Avastin seul et Campto- Avastin, de l’essai AVF3708G, les toxicités de niveaux 1 à 4 étaient l'hémorragie (40%), l'hypertension (32%), le nez qui saigne (26%), les caillots de sang dans les veines (8%), les caillots de sang dans les artères (6%), les complications de la cicatrisation (6%), les saignements dans le cerveau (5%), les protéines dans les urines (4%), la perforation gastro-intestinale (2%). Chez les 82 malades traités avec Campto-Avastin, les niveaux de toxicité de 3 à 5 ont été des caillots de sang dans les veines (7%), l'hypertension (5%), les caillots de sang dans les artères (3%), les complications de la cicatrisation (3%), la perforation gastro-intestinale (2%), l'hémorragie (2%), le saignement dans le cerveau (1%) et les protéines dans les urines (1%). On a observé des saignements intracrâniens chez 8/163 malades. 2/8 patients avaient le niveau 3 et 4. Chez les patients avec le saignement sérieux ou l'hémoptysie récente, Avastin a été suspendu.
GFME : 271
Des nano capsules d'Indométacine réduisent le glioblastome in vivo chez le rat
La thérapie d'anticorps monoclonaux ciblés avec la radiothérapie et la chimiothérapie peut augmenter l'efficacité des traitements anti tumoraux. Mais les gliomes récidivent ou progressent rapidement malgré les traitements et deviennent vite envahissants. Les nanoparticules de polymères ont provoqué un intérêt grandissant ces dernières années dans la livraison de médicaments anti tumoraux car ils peuvent fournir une livraison soutenue, contrôlée et bien ciblée. Des nano capsules d'Indométacine ont été introduites dans un modèle de gliome expérimental chez le rat. Le résultat a montré une réduction considérable dans la dimension de la tumeur avec la moitié des animaux qui ne présentaient après le traitement que quelques cellules résiduelles de tumeur. Les analyses pathologiques ont montré une réduction considérable dans l'index mitotique de prolifération et d'autres caractéristiques histologiques qui indiquent un tumeur moins invasive et proliférative. La livraison d'Indométacine par les nano capsules a réalisé des plus hautes concentrations intracérébrales de médicament que la concentration habituelle d'Indométacine en solution. On a observé une plus grande concentration dans l'hémisphère où le gliome avait été implanté, comparée avec l'autre hémisphère controlatéral sain. Le traitement de nano capsules d'Indométacine n'a pas causé de toxicité et a augmenté la survie des animaux. Ces données suggèrent que les nano capsules d'Indométacine pourraient offrir de nouvelles stratégies potentiellement très efficaces dans le traitement des gliomes malins.
Référence Pubmed : 19286307 et GFME : 270
DMC, un nouveau médicament prometteur qui inhibe l’angiogenèse
On connait tous l’intérêt que portent les malades avec glioblastome aux Etats-Unis à l’anti-inflammatoire Celebrex, un inhibiteur de Cox 2. Des Chercheurs à l'Université de Californie Du sud ont identifié un nouveau médicament qui paraît cibler typiquement les cellules tumorales et la croissance des vaisseaux sanguins environnants sans les effets secondaires négatifs associé aux inhibiteurs de Cox-2. Ce produit, le DMC, 2.5-diméthyle-celecoxib (DMC) paraît avoir un fort effet anti tumoral en réduisant la provision de sang nécessaire pour la croissance de la tumeur, d'après les données présentées à la 100ème réunion annuelle 2009 de l'AACR. Les conclusions ont été présentées le 19 avril 2009. Le traitement qui parait prometteur en traitement à long terme n'a pas les effets cardio-vasculaires négatifs associés avec les inhibiteurs de Cox-2. DMC a une activité antitumorale sans inhibition de Cox-2 et le risque augmenté associé de complications cardio-vasculaires. Ce médicament est cytotoxique pour les cellules de l'endothélium vasculaire, associé à un étouffement de la prolifération cellulaire et la migration sans effets toxiques apparents aux tissus normaux. La thérapie dans les études animales a montré une réduction des tumeurs et une moins grande densité des vaisseaux sanguins dans les tumeurs, 35 à 40% de réduction dans la densité des vaisseaux sanguins.
Les premiers résultats allemands de Temodal et ions carbone sur deux lignées de glioblastomes, encourageants
Des lignées de cellules de glioblastome U87-MG exprimant la forme sauvage de p53 (p53 Wild type) et LN229 exprimant simultanément la forme mutée et sauvage de p53 (Wilde+mutant) ont été irradiées avec des ions carbone mono énergétiques de transfert d'énergie linéaire (LET) de 172 keV/mum avec un pic de Bragg étendu atteint au maximum LET de 103 keV/mum après traitement avec 10 muM ou 20 muM de Temodal. La cytotoxicité a été mesurée par l'examen de la survie, l'augmentation cellulaire ainsi que la progression du cycle cellulaire.
Les cellules avec la forme mutée de p53 étaient plus sensibles à l'irradiation par ions carbone que les cellules avec la forme sauvage de p53 qui a aussi été observé par une phase G2 plus courte. Les ions carbones ont montré une efficacité biologique augmentée dans les deux lignes cellulaires. La ligne cellulaire LN229 a été plus sensible au traitement avec Temodal que la lignée U87MG qui exprimait la forme sauvage de p53. La combinaison de Temodal et de l'irradiation par ions carbone a montré un effet additif dans les deux lignes cellulaires. L'irradiation par les ions carbone est considérablement plus efficace pour ces lignées cellulaires de glioblastome que la radiothérapie classique par photon. Un traitement supplémentaire avec Temodal peut offrir une grande chance dans le traitement des glioblastomes. Bientôt proposé à Lyon.
Référence : International Journal of Radiation Biology février 2009. GFME : 264
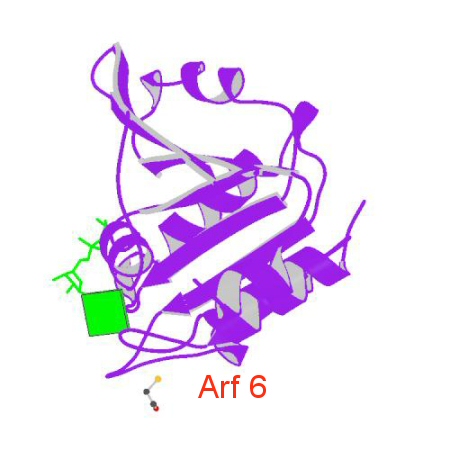
ADP-ribosylation facteur 6 ou ARF6 règle l'invasion cellulaire des gliomes à travers l'IQ-domain GTPase-activating protein 1 par la médiation de RAC 1
Ce qui caractérise les gliomes malins, c'est l'infiltration insidieuse des cellules tumorales dans le parenchyme du cerveau, rendant ces tumeurs mortelles et pratiquement incurables avec les thérapies disponibles. ADP-ribosylation facteur 6 ou ARF6, est un membre de la famille des ADP-ribosylation facteur, elle-même une partie de la superfamille RAS, abondamment exprimé dans les cellules du gliome humain envahissantes. Un épuisement cellulaire d'ARF6 par un petit ARN importun a diminué l'activation de Rac1, HGF-Stimulé et sérum-stimulé du gliome, et affaibli la migration cellulaire in vitro, diminuant d'une façon marquée la capacité envahissante des gliomes à envahir le cerveau. En outre, l'expression anormale d'ARF6 dans les cellules du gliome a encouragé la migration cellulaire par l'activation de Rac1. Sur la stimulation des cellules de gliome avec HGF, IQGAP1 (IQ-domain GTPase-activating protein 1) est recruté et se chevauche avec ARF6 à la pointe des cellules migrantes. Cependant, l'épuisement cellulaire d'ARF6 a abrogé ce recrutement d'IQGAP1 et a atténué la formation de sorties de la surface. ARF6 forme des complexes avec Rac1 et IQGAP1 dans les cellules de gliome sur stimulation d'HGF, et le knock-down d'IQGAP1 inhibe considérablement l'activation de Rac1, ARF6-Induite et la migration des cellules. L'activation de Rac1 avec ARF6 en médiateur est essentielle pour l'invasion cellulaire des gliomes par un chemin de signalisation qui exige IQGAP1.
Référence : 19155310 et GFME : 262.
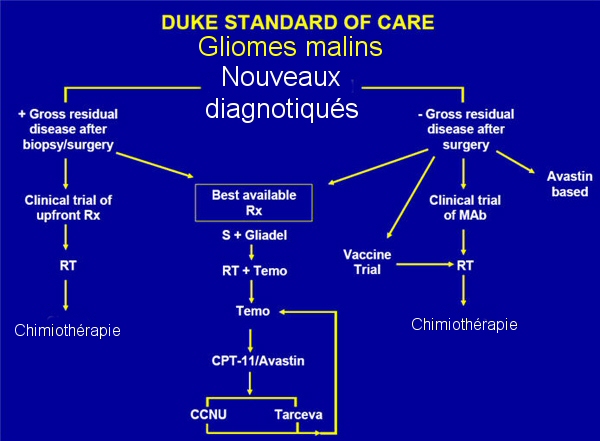
Comment soigne-t-on au DUKE ?
De 2003 à 2006, le traitement standard au Duke était la chirurgie(85%) avec Gliadel, 42,3% et non Gliadel 57,6% puis la radiothérapie avec Temodal suivi de Temodal puis CCNU, puis Campto (Iritonecan) pendant 1 an et retour au cycle Temodal, CCNU, Campto toujours pour 1 an. Pour les patients ayant reçu Gliadel, Survie à 2 ans de 43% et 90 semaines de survie moyenne. Sans Gliadel, survie de 27% à 2 ans et 72 semaines de survie moyenne.
Depuis 2007, le traitement standard est toujours la chirurgie avec ou sans Gliadel, suivi de la radiothérapie avec Temodal, suivi de Temodal, puis de Campto-Avastin, puis de CCNU et Tarceva et retour au Temodal.
Les meilleurs hôpitaux français ne proposent pas autre chose, sauf peut être BICNU au lieu de CCNU sans Tarceva car en France les patients n’ont qu’une confiance limitée dans les chimiothérapies orales.
On propose aussi plusieurs essais cliniques, des vaccins, Neuradiab.
Quel traitement après l’échec d’Avastin ?
Selon les résultats que nous avons analysés de l’ASCO, c’est Glivec -Hydrea-Tarceva qui obtient la palme.
Aux Etats-Unis, c’est CCNU-Tarceva qui a les préférences
En France c’est BICNU, seul, qui a la préférence.
Qui a dit ?
Les malades avec glioblastome ne sont pas universellement incurables, avec une fraction toujours croissante, bien que petite, de malades qui paraissent survivre à la maladie. L'utilisation de chimiothérapies multiples avec des toxicités qui ne se chevauchent pas et des mécanismes d'action indépendants produit une cohorte toujours croissante de malades pour qui le glioblastome n'est pas un événement terminal.
Professeur Henry S Friedman, neuro-oncologue au Preston Robert Tisch Brain Center Duke, Durham, Caroline du Nord en 2007, numéro 1 mondial.
http://www.cancer.duke.edu/btc/
Les cellules gliales et la chirurgie des gliomes
Les cellules gliales ont été découvertes il y a 118 ans, en 1891 par un médecin espagnol Ramon y Cajal qui reçut pour sa découverte le prix Nobel en 1906.
La première opération d’un gliome eut lieu il y a 125 ans, le 25 novembre1884 par le chirurgien anglais Ricman Godlee anobli en Sir Rickman sur un jeune paysan anglais de 25 ans, John Mitchell qui ne survivra qu’un mois.
Les études françaises présentées à l’ASCO 2009
Deux études françaises sont présentées cette année au congrès mondial de l’oncologie (ASCO). La première étude de La Salpêtrière est présentée par le Dr. Sophie Taillibert et concerne le régime Campto-Avastin sur oligodendrogliomes anaplasiques. La seconde étude de La Timone à Marseille, présentée par le Pr. Olivier Chinot concerne un biomarqueur d’activité tumoral sous Campto-Avastin, u-PA (urokinase Activator Plasminogène), à partir d’une simple prise de sang, un indicateur assez voisin de celui de l’hôpital Presbytérien de New-York.
Bravo à nos deux meilleures équipes françaises.
Toutes les présentations de l'ASCOO 2009
Source
Les derniers essais cliniques en cours
1-(3/09) France, essai EORTC, La Salpêtrière, La Timone, radiothérapie contre chimiothérapie sur gliome de bas grade, stratification selon statut 1p.
2-(4/09), E-U, glioblastome en récidive, Temodal et Avastin toutes les 2 semaines, Avastin, 10 mg/kg, jours 1 et 15/28 jours et Temodal, 100mg/m2, jours 1-5 et 15-19/28 jours. Renseignements sur le site officiel http://clinicaltrials.gov
3-(3/09), E-U, Neuradiab, de l’iode radioactif, 44 grays, I-131 à l’emplacement de la tumeur retirée en complément de la radio chimiothérapie standard de Temodal sur glioblastome nouveau (III).
4-E.U. (4/09) Tandutinib (MLN518), un inhibiteur de tyrosine kinase (I/II).
5-France-La Salpêtrière, Europe et Etats-Unis, NovoTTF-100A, un appareil portable avec batterie qui alternent les champs électriques pour bloquer la division cellulaire, pour glioblastome récurrent ou progressif (III randomisé et donc tirage au sort).
6-E-U (4/09),Trabectédine (Yondelis), une nouvelle chimiothérapie pour enfants et adolescents avec tumeur solide réfractaire (I).
7-E-U (5/09), Interféron Alfa-2b (PEG INTRON) pour enfants avec gliome malin du tronc cérébral.
8-E-U (3/09), Iritonecan liposomial (NL CPT 11) sur glioblastome en récidive (I)
Ils nous ont quittés
Ils ont encore été très nombreux à nous quitter depuis le début de l’année 2009.
-Le 09/07/2008, Francisco, le mari de Fernanda.
-Le 26/01/2009, Jean-Elie, 69 ans, le mari de Martine.
-Le 28/01/2009, Evelyne 52 ans, la maman de Sonia.
-Le 14/1/2009, le mari de Micheline
-Le 15/01/2009, Charles, 44 ans, le mari d’Isabelle.
-Le 17/01/2009, Louis 78 ans, le papa de Francine.
- Le 19/01/2009, Nathalie, 24 ans, l'amie d'Alexandre
-Le 30/01/2009, Alain, le frère d’Edith.
-Le 30/01/2009, Jeannine, 75 ans, la maman de Marie-Noëlle
-Le 16/02/2009, Liliane, 52 ans, l’épouse de Jean-Claude.
-Le 05/03/2009, Jean-Louis, 62 ans, le mari de Marie-Madeleine.
-Le 18/03/2009, Nino, 6 ans, le fils de Christophe et Elodie
-Le 24/03/2009, Jean-Claude, 66 ans, le mari de Françoise.
-Le 30/03/2009, Florence, 59 ans, la maman d’Aude.
-Le 08/04/2009, Josette, 64 ans, la maman de Katia.
-Le 19/04/2009, Damien, 34 ans, le fils d’Annie
-Le 22/04/2009, Dominique, 57 ans, le mari de Catherine
-Le 01/05/2009, Sébastien, le beau-frère de Muriel, le papa de Kevan 3ans et Emily 1 an.
-Le 9/05/2009, Paulette, 61 ans, la maman de Christine et Isabelle.
A toutes les familles, GFME adresse ses plus sincères condoléances.
Mailing-listes, des adhérents toujours plus nombreux
Nous avons désormais dépassé les 500 adhérents sur les 2 mailing-listes, 505 contre 489 le trimestre dernier (+3,3%). 330 inscrits sur la liste gfme contre 318 le trimestre dernier (+3,8%) et 175 sur la liste astrocytome-gfme contre 171 (+2,%) le trimestre dernier. Le succès démontre avec les messages de plus en plus nombreux l’utilité de ces listes de discussion pour les familles de patients qui y trouvent des réconforts et des soutiens.
Le site Internet, toujours en progression autour 1000 visites/jour

Le site Internet a 2 adresses
http://gfme.free.fr/
http://gfme.fr/
La fréquentation du site en forte croissance depuis 2006 reste désormais stable comparée à 2008. Pour les quatre premiers mois de 2009 comparés aux quatre premiers mois de 2008. 29806 visiteurs en 1/09, 29559 en 2/09, 32689 en 3/09 et 28334 en 4/09 soit 120388 visiteurs au total contre 29287 en 1/08, 26860 en 2/08, 30592 en 3/08, 32883 en 4/08 soit 119622, un nombre équivalent
Semaine mondiale contre les tumeurs cérébrales organisée par IBTA
Elle aura lieu cette année du 1er au 7 novembre avec une marche à Marseille le samedi 7/11.
***************************
Rendez-vous pour le prochain numéro, le n° 16 en septembre-octobre 2009.
Glioblastome Association
Michèle Esnault (GFME)
Bât a, 22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 euros. Renouvellement 7,5 euros, reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N