GFME bulletin n°51
Suite

Glioblastome Association Michèle Esnault (GFME) Bât A, boîte 4, 22 bd Camille Flammarion 13001 Marseille
Recevoir gratuitement par courrier le bulletin à domicile
Télécharger ce bulletin n° 51 en .pdf

Cliquer pour agrandir
Docteur Emeline TABOURET Maître de conférence, Praticien hospitalier Hôpital de la Timone
Le mot du président
J’ai mis, en photo de ce numéro, une jeune marseillaise, le Dr Emeline TABOURET qui vient d’obtenir un poste de Maître de conférence-Praticien hospitalier à l’hôpital de la Timone de Marseille. Emeline a passé un an aux Etats-Unis de fin août 2017 à août 2018 au sein du NIH, National Instituts of Health (santé), institut étant au pluriel car il y en a 20 en réalité, le 1er ayant été crée en 1937, le NIH et le dernier en 1956, la NLM, tous financés par des fonds publics. En plus des 20 instituts il y a 7 centres de recherche avec des noms différents, CIT, CSR, NCCAM… 18000 personnes dont 6000 chercheurs y travaillent pour un budget annuel de 30 milliards de dollars. C’est une immense structure scientifique dans la petite ville du Maryland (côte ouest au sud et pas loin de New-York), Bethesda. Emeline a travaillé sur les cellules souches tumorales et a réalisé un projet de recherche sur l’évaluation d’un nouveau médicament contre le glioblastome. Elle a rencontré des collègues de très haut niveau, des Chinois, des Coréens et découvert d’autres cultures, d’autres méthodes de travail. Au dernier congrès de la société européenne d’oncologie ESMO à Munich le 25/10/2018 elle a fait une exposition très remarquée sur la nouvelle classification OMS des tumeurs gliales que j’ai pu regarder sur le site https://www.mediscoops.net, dont j’ai extrait la photo.
Bravo Emeline
Bonne et heureuse année 2019 à tous
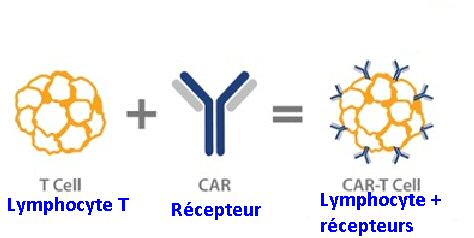
L’année 2018 n’a pas apporté de grandes améliorations dans le traitement des glioblastomes dont la survie reste faible. Il y a de grands espoirs avec le traitement à long terme de temozolomide + anti PD1 sur des modèles murins éliminant complètement le glioblastome chez la souris. Il reste aussi les CAR-T Cells, lymphocytes modifiés génétiquement pour leur apprendre à repérer les cellules cancéreuses et à les tuer ou les faire manger par les macrophages cérébraux. Ces traitements CAR-T ou d’association chimiothérapie + immunothérapie seront-ils remboursés ? On l’espère et nous devons les essayer et garder confiance en l’avenir. Au nom des malades, je remercie tous les professionnels de santé au contact des malades avec des tumeurs de cerveau de tous grades qui chaque jour se dévouent, souvent sans compter leur temps, pour trouver aux malades les meilleurs traitements, un accueil adapté et soulager des familles très souvent effondrées. Félicitations et merci à tous.
Les oncologues sont en colère, une perte théorique de chance thérapeutique avec des médicaments non remboursés en association avec l’immunothérapie
Alors que la connaissance avance, de nouvelles associations de molécules améliorent le pronostic des cancers les plus graves mais ne peuvent être utilisées pour un problème de coût. Des études récentes ont mis en évidence l’efficacité de l’association immunothérapie + chimiothérapie contre plusieurs cancers, rein, sein, ovaires. Pour le cancer du sein triple négatif l’immunothérapie d’atezoluzumab + la chimiothérapie de nab-paclitaxel (Abraxane) donne de très bons résultats, mais cette chimiothérapie n’est pas remboursée en association. Le Pr. Khe-Hoang-Zuan de la Salpêtrière, Directeur de l’Anocef m’a fait part que le bevacizumab plus connu sous son nom commercial Avastin (AMM pour la DMLA) du grand laboratoire Suisse Roche, ne serait plus remboursé s’il est prescrit comme aux Etats-Unis en récidive de glioblastome. GFME a demandé à notre Ministre Agnès BUZIN, ex directrice de l’Institut National du Cancer de maintenir ce remboursement pour nos malades avec glioblastome récurrent car actuellement le traitement le plus efficace.
Un robot de neuro-chirurgie, ROSA, à La Timone à Marseille
Après 3 ans de négociation, un robot de neuro-chirurgie flambant neuf est arrivé à Marseille dans le service du Professeur Jean Régis à l’hôpital de la Timone à Marseille. Ce robot permet une plus grande précision et une meilleure sécurité des gestes opératoires en chirurgie stéréotaxique. On l’utilise pour les biopsies et pour certains types de tumeurs cérébrales. Début octobre les premiers patients ont pu en bénéficier. L’achat a été financé privé et public APHM, département des Bouches-du-Rhône, Entreprises, ARTC Sud.
Actualité 668 16 septembre 2018 cliquer ici
L'inhibition de la PLK1 cible les cellules de gliome malin activées par Myc, quelle que soit la résistance acquise au temozolomide liée à une déficience liée à la réparation de l'appariement.
C’est une grande équipe de Harvard qui publie cette intéressante étude en constatant que la déficience en réparation du mésappariement (MMR) par inactivation de MSH6 a été identifiée dans 30% des gliomes récurrents de haut grade et représente un mécanisme moléculaire essentiel à la base de la résistance acquise au temozolomide. L'inhibition de la PLK1 induit une catastrophe mitotique, un arrêt du cycle cellulaire G2 / M et des lésions de l'ADN, conduisant à une apoptose médiée par la caspase dans le glioblastome. L'inhibition de PLK par le volasertib a inhibé efficacement la croissance tumorale de xénogreffes de glioblastome résistantes au temozolomide et représente une nouvelle option thérapeutique pour les gliomes récurrents, dont ceux résistants au temozolomide.
Actualité 669 26 septembre 2018 cliquer ici
Expression de LAG-3 (CD 223) et efficacité d’un traitement combiné avec des anticorps monoclonaux anti-LAG-3 et anti-PD-1 dans le glioblastome
C’est une grande équipe de Johns Hopkins et de BMS qui s’intéresse à l’immunothérapie et à un nouvel inhibiteur du point de contrôle immunitaire, LAG-3, qui est exprimé dans le glioblastome humain. LAG3 est une abréviation de Lymphocyte Activation Gene-3, qui supprime la réponse immunitaire par des effets directs sur les cellules T CD8 +. Le blocage simultané de LAG-3 et de PD-1 peut restaurer l'activation des lymphocytes T et renforcer l'immunité antitumorale. LAG-3 est aussi un marqueur précoce de l'épuisement des cellules T et un traitement précoce par un anticorps bloquant LAG-3 comme BMS-986016 est plus efficace qu'un traitement ultérieur. Ces données appuient des essais cliniques sur le glioblastome.
Actualité 676 du 18 décembre 2018 ***** cliquer ici
Effet du traitement combiné anti-PD-1 et temozolomide dans le glioblastome
Ce sont les Coréens qui étudie l’association temozolomide + immunothérapie anti PD1 qui sur les souris élimine les glioblastomes définitivement. Ils ont évalué les effets thérapeutiques de l'anti-PD-1 + temozolomide dans un modèle de glioblastome orthotopique murin. Le nombre et la composition des lymphocytes ont été évalués par cytométrie en flux. La génération d'une mémoire immunologique antitumorale a été étudiée lors d'un nouvel essai thérapeutique. Le traitement combiné anti-PD-1 + temozolomide a permis d'obtenir une efficacité antitumorale synergique en présence de lymphocytes T PD-1 + et CD8 +. Alors que le temozolomide n'a pas sauvé les souris implantées avec glioblastome, l'anti-PD-1 a complètement éradiqué le glioblastome chez 44,4% des souris et la combinaison anti-PD-1 + temozolomide chez toutes les souris. L'anti-PD-1 augmente le nombre de lymphocytes infiltrant la tumeur (TILs) et réduit la fréquence des lymphocytes T épuisés et des lymphocytes T régulateurs. Cependant, le temozolomide + l'anti-PD-1 a réduit le nombre de TILs, ce qui est observé aussi avec le temozolomide seul. Une analyse du transcriptome des tissus tumoraux a révélé que la monothérapie anti-PD-1 perturbait les gènes liés au système immunitaire, de manière distincte de la thérapie combinée. En conclusion, le blocage de PD-1 induit une réponse thérapeutique à long terme et la combinaison avec le temozolomide augmente encore l'efficacité antitumorale. Cependant, la mémoire immunologique est provoquée par la monothérapie anti-PD-1 et non par la thérapie combinée.
Pubmed : 30546966.
Actualité 671 24 octobre 2018 cliquer ici
Traitement intra-tumoral avec oxygène-ozone dans le glioblastome
Ce sont plusieurs équipes allemandes qui s’associent pour étudier l’action de l’ozone sur le glioblastome. Après une chirurgie associée à une radiochimiothérapie standard, de l'O2-O3 (5 ml à 40 µg / ml) a été appliqué toutes les 4 semaines dans la zone tumorale. Les patients ont reçu une médiane de 27 applications O2-O3 (gamme 3-44). Le taux de survie globale médian était de 40 mois (gamme 16-53 mois). Le taux de survie médian après la première récidive ou l’initiation du traitement par O2-O3 était respectivement de 34 mois (gamme 12-53 mois). Ces données confirment les avantages potentiels d'une application intra-tumorale d'O2-O3 dans les glioblastomes récurrents. Les équipes considèrent que l’ozone, O3, pourrait être considéré comme un traitement adjuvant viable pour les patients.
Actualité 672 08 novembre 2018 cliquer ici
La faible toxicité tardive chez les survivants à long terme d'une étude de phase 2 sur la radiothérapie simultanée avec le temozolomide et l'acide valproïque chez le glioblastome récemment diagnostiqué
C’est une équipe du NIH de Bethesda où est resté 1 an Emelyne Tabouret qui publie la toxicité tardive de la depakine associée à la radio-chimiothérapie de temozolomide pour glioblastome. L'acide valproïque (Depakine) est un antiépileptique doté d'une activité inhibitrice de l'histone déacétylase qui améliore la survie globale et la survie sans progression chez les patients présentant un glioblastome récemment diagnostiqué. 37 patients atteints d'un glioblastome nouvellement diagnostiqué ont reçu le traitement d'association. Les toxicités tardives ont été évaluées chez 6 patients ayant vécu plus de 3 ans. La durée médiane de suivi pour ces 6 patients était de 69,5 mois. Dans cette cohorte, la survie totale médiane était de 73,8 mois (60,8 mois -103,8 mois) et la survie sans progression médiane de 53,1 mois (37,3 mois- 103,8 mois). La toxicité tardive était neurologique, douleur, mais aussi sanguine, de la moelle osseuse. La plupart des toxicités étaient de niveau 1/2 et seulement 2 toxicités de niveau 3/4. L’ajout d'acide valproïque à la radiothérapie + temozolomide chez les patients atteints de glioblastome nouvellement diagnostiqué a été bien toléré avec une faible toxicité tardive. En outre, l'acide valproïque peut entraîner de meilleurs résultats par rapport aux données historiques et mérite une étude plus approfondie.
Pubmed : 30402263
Actualité 673 14 novembre 2018 cliquer ici
Les empreintes immunitaires globales dans le sang périphérique d'un patient atteint de glioblastome révèlent des signatures d'immunodépression associées au pronostic
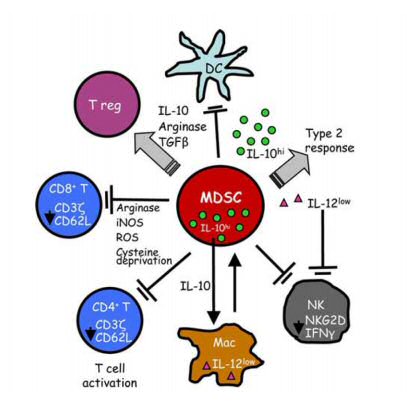
sont plusieurs équipes, Cleveland Clinic, du Danemark, du Brésil qui s’associent pour constater que le glioblastome reste uniformément létal et ce, malgré une importante accumulation de cellules immunitaires dans le microenvironnement et que la réponse immunitaire antitumorale est limitée. Une meilleure compréhension de la réponse immunitaire des glioblastomes au cours de la progression de la maladie est donc nécessaire. En utilisant l'analyse par cytométrie de flux dans une cohorte de 259 patients allant de tumeurs cérébrales primitives et métastatiques bénignes à malignes, on constate que les patients avec glioblastome présentent une élévation significative du nombre de MDSCs, cellules suppressives myéloïdes dans le sang périphérique mais non dans les Tregs immunosuppresseurs. Dans le tissu du patient glioblastome, on constate que l'augmentation des niveaux de MDSCs dans les cas récurrents de glioblastome laissent présager un mauvais pronostic. L'analyse du sang périphérique des patients avec glioblastome nouvellement diagnostiqué révèle une réduction des MDSCs avec le temps qui s'accompagne d'une augmentation concomitante des CD (cellules dendritiques). Les patients glioblastome avec une survie prolongée avaient également un nombre réduit de MDSCs, similaire aux taux des patients atteints de gliome de bas grade (LGG). Cela justifie une stratégie visant à cibler les MDMCs, qui sont élevées chez les patients avec glioblastome et qui prédisent un mauvais pronostic.
Pubmed : 30385717
Actualité 674 17 novembre 2018 cliquer ici
Les lymphocytes T CAR ciblant l'intégrine α v β 3 sont efficaces contre le cancer avancé dans les modèles précliniques
Ce sont nos amis allemands qui s’intéressent après les cellules dendritiques aux T-CAR pour viser les intégrines qui sont des récepteurs hétérodimères qui véhiculent des interactions cellule à cellule et cellule à matrice. L'intégrine α v β 3 est exprimée dans plusieurs entités tumorales, le mélanome, le glioblastome, les cancers du sein, du pancréas et de la prostate, où elle favorise la survie des cellules tumorales et les métastases. Ils ont mis au point des cellules T de récepteurs d'antigènes chimériques (CAR) spécifiques à α v β 3 et analysé leur fonction antitumorale dans des modèles précliniques in vitro et in vivo. Les lymphocytes T-CAR α v ß 3 ont bien éliminé les cellules tumorales α v β 3 + rapidement et précisément par production d'IFN-γ et d'IL-2 (CD4 + et CD8 + ) et de plus présentait une prolifération productive. In vitro ils observent une forte réactivité avec la hLM609v7 d'affinité α v ß 3 -CAR dans la configuration courte d'espacement. Avec une seule administration de hLM609v11 αv, les cellules T β 3 -CAR étaient capables d'induire une élimination complète de mélanome et une survie à long terme sans tumeur. Ces données établissent l'intégrine α v β 3 comme nouvelle cible de l'immunothérapie par cellules T CAR et confirme l’idée selon laquelle l'affinité du domaine de liaison et la longueur de l'espaceur peuvent être calibrées pour augmenter la réactivité de la CAR.
Pubmed : 30420973
Actualité 675 du 5 décembre 2018 cliquer ici
L'expression de PD-1 par les cellules T chez les patients atteints de gliome malin reflète l'épuisement et l'activation
C’est une équipe mixte californienne et allemande qui étudie le rôle de PD1 sur les lymphocytes. De récents travaux précliniques suggèrent que PD-1 / PD-L1 joue un rôle immunorégulateur important pour limiter les réponses des cellules T antitumorales efficaces induites par une immunothérapie active. Cependant, le rôle fonctionnel que joue PD-1 sur les lymphocytes T humains chez les patients atteints de gliome malin est mal connu. Ils ont découvert plusieurs différences entre les lymphocytes infiltrant la tumeur (TILs) PD-1 + et les lymphocytes T PD-1 + du sang périphérique. Les lymphocytes ayant infiltré la tumeur (TILs PD-1 + ) présentaient une expression plus élevée de marqueurs d'activation et d'épuisement que les cellules T PD-1 + du sang périphérique, qui avaient plutôt des marqueurs de mémoire plus importants. Une comparaison des populations de chaînes variables du récepteur des lymphocytes T a révélé une diminution de la diversité des lymphocytes T exprimant PD-1, quel que soit le lieu obtenu. Sur le plan fonctionnel, les cellules T PD-1 + du sang périphérique avaient une capacité de prolifération lors de l'activation considérablement accrue par rapport aux cellules T PD-1-. Ces preuves suggèrent que l'expression de PD-1 chez les patients atteints de gliome reflète des lymphocytes T effecteurs activés de manière chronique qui affichent des caractéristiques de mémoire et d'épuisement en fonction de leur emplacement anatomique. La diversité réduite des cellules T PD-1 + suggère que la population exprimant PD-1 a une gamme plus étroite de cibles d'antigènes apparentés par rapport à la population sans expression de PD-1. Cette information peut être utilisée pour expliquer les réponses immunitaires aux thérapies de blocage de PD-1 ou à d’autres immunothérapies.
Pubmed : 30498094
Oscar Lambret a été l’ami de Roger Salengro, Maire de Lille, Ministre (Lille 1890-1936-suicide)
Le Pr. Oscar Lambret est un grand chirurgien créateur du centre anticancéreux de Lille qui porte son nom. Né en 1872 à Avesnelles, dans le département du Nord, petit village proche de Maubeuge et de la frontière Belge. Il fait ses études au lycée de Douai puis des études de Médecine à la Faculté de Lille. Il est reçu au concours d'internat en 1893 à 21 ans. 2 ans plus tard, en 1895 il est chef de clinique dans le service de chirurgie de l'hôpital Saint-Sauveur. Reçu à l’agrégation de chirurgie, à 29 ans en 1901, d’une grande habileté, il devient chef du service chirurgie de Saint-Sauveur, en 1907 à 35 ans. Elu membre de la commission administrative des hospices civils, puis en 1926, vice-président, il a l’idée avec le maire de Lille, Roger Salengro, de créer une grande cité hospitalière et universitaire dont le projet est confié à l'architecte américain Paul Nelson avec une forme rayonnante d’un anneau géant avec une double étoile à 5 branches. La construction débutée en 1936 s’interrompt pendant la guerre en 1939. Le Pr. Lambret, souhaite aussi la construction d'un hôpital dédié à la lutte contre le cancer et d’un institut de recherche. Ce centre anticancéreux qu’il dirigera est situé au fond du jardin de l'hôpital Saint-Sauveur. Membre influent de l'Académie de Chirurgie, il est prolongé dans ses fonctions en raison de la guerre et décède le 17 octobre 1943 à l'âge de 71 ans. C'est le Pr. Delannoy qui lui succède comme chirurgien de l'hôpital Saint-Sauveur qui inaugurera en 1953 le premier service de Chirurgie de la Cité Hospitalière rêvé par le Pr. Lambret. Son successeur au Centre anticancéreux, le Pr. Driessens fera aboutir en 1955 le projet d'un nouvel hôpital de 300 lits dénommé Centre Oscar Lambret. Le centre est dirigé depuis 2016 par le professeur Eric Lartigeau.
Source : wikipédia
Les derniers essais en cours d’après le site Clinicaltrials
1- (11/2018), Phase I/II, Allemagne, Heidelberg, combinaison de VXM01 et d'un inhibiteur de point de contrôle anti-PD-L1, Avelumab pour glioblastome progressif résécable et non résécable.
VXM01 de Merck est un vaccin peptide ciblant VEGFR2, vaccin à base de lymphocytes T spécifique du VEGFR2. Avelumab est un inhibiteur PD-L1.
2- (09/2018), Phase II, Etats-Unis, Dana-Farber,
Pembrolizumab + ré-irradiation de glioblastome récurrent naïf de bevacizumab ou résistant au bevacizumab.
Le pembrolizumab ou Keytruda est un inhibiteur Merck de PD1 (les tumeurs expriment le récepteur PD-L1). La radiothérapie et l’immunothérapie donnent parfois de bons résultats car la radiothérapie dilate la barrière hémato-encéphalique pour mieux laisser passer les médicaments et les lymphocytes T.
3 - (09/2018), Phase II, Etats-Unis, Dana-Farber (Pr. Reardon) et d’autres
hôpitaux, pembrolizumab + bevacizumab + ré-irradiation.
Le pembrolizumab (200 mg) sera administré par voie intraveineuse (IV) 1 fois toutes les 3 semaines puis 1 fois toutes les 4 semaines et 1 fois toutes les 6 semaines. Le bevacizumab (15 mg / kg) sera administré par voie intraveineuse (IV) 1 fois toutes les 3 semaines. La ré-irradiation (35 Gy) sera administrée aux patients 5 jours par semaine pendant 2 semaines. Même les bas grades sont éligibles.
4 - (11/2018), Phase II, Etats-Unis, Memorial Sloan - Kettering Cancer, Nivolumab + ré-irradiation + bevacizumab pour glioblastome récurrent MGMT méthylé.
Le nivolumab ou Opdivo est un inhibiteur PD-1 qui sera administré à raison de 3 mg / kg par voie intraveineuse avant la ré-RT, jours 1 et 14 et avec le bevacizumab aux jours 28, 42 et 56. La ré-irradiation commencera au jour 28 pour 5 fractions de 600cGy tous les 2 jours sur une période de 2 semaines. Le bevacizumab sera pris dès le début de la ré-RT et à raison de 10 mg/kg en intraveineuse les jours 28, 42 et 56. Après le jour 56, de nouvelles doses de bevacizumab pourront être administrées toutes les 2 semaines.
5 - (07/2018), Phase2, Etats-Unis, Duke pour gliome de haut grade (III et IV) nouvellement diagnostiqué, radiothérapie concomitante avec temozolomide + BMX-001 (BMX-HGG)
BMX-001 a été mis au point à Duke. Associé à la radiothérapie il provoque une réaction différentielle qui protège la cellule normale tout en aidant à tuer la cellule tumorale.
6-(06/2018) Phase II, Sterimgli, RST, radiothérapie stéréotaxique hypofractionnée seule ou RST + durvalumab anti-PD-L1 d’Astrazeneca pour glioblastome récurrent.
Cet essai est actuellement centralisé Par la Pr. Elisabeth MOYAL à Toulouse, mais la plupart des CLCC le proposent ainsi que quelques CHU comme La Salpêtrière
Ils nous ont quittés
-Le 05/12/2018, Michel, 67 ans, le papa de Sylvie
Sites Internet, mailing-listes, Facebook entre le 01/09/2018 et le 30/11/2018
GFME apparait en 3ème position si on saisit glioblastome sur Google. Chez Free 46767 visites en octobre soit 1508 visites/jour et 42279 en novembre 2018 soit 1409 visites/jour. A ces visites s’ajoutent toutes celles chez 1 et 1 avec 5 noms de domaine.
Parmi les mots saisis, c’est plaquettes, norme, qui arrive largement en tête et GFME apparait en tête de recherche sur ces 2 mots.
Les 2 mailing-listes de GFME et Facebook
La page Facebook de GFME est très fréquentée et je l’actualise souvent. On peut aussi m’y poser des questions.
https://www.facebook.com/GFME-273113652709280/
Les mailing-listes ont toujours de nombreux adhérents, mais peu de messages.
La mailing-liste gfme@yahoogroupes.fr qui a été créée le 15/08/2002 compte 440 membres contre 437 le trimestre dernier, en progrès. 7 messages en octobre, 1 seul en novembre. La liste astrocytome-gfme@yahoogroupes.fr , compte 280 membres contre 278 le trimestre précédent en progrès aussi, 1 message en octobre et 1 en novembre, ce n’est pas beaucoup.

Rendez-vous pour le prochain numéro, le n° 52 en Avril 2019
Glioblastome Association
Michèle Esnault (GFME)
Bât A, boîte 4
22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 €/Renouvellement 7,5 €.
Reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N
Michèle Esnault Fondatrice de GFME en 2001 (16 ans)