GFME bulletin n°49
Suite

Glioblastome Association Michèle Esnault (GFME) Bât A, boîte 4, 22 bd Camille Flammarion 13001 Marseille
Recevoir gratuitement par courrier le bulletin à domicile
Télécharger ce bulletin n° 49 en .pdf

Cliquer pour agrandir
Professeur Elisabeth MOYAL, radiothérapeute à l'Oncopole-Radiopole de Toulouse
IUCT Oncopole
1 avenue Irène Joliot-Curie
31059 Toulouse Cedex.
Le mot du président
J’ai mis, en photo de ce numéro, l’une de nos meilleures spécialistes en immunothérapie des cancers, le Pr. Elisabeth MOYAL, radiothérapeute à l’Institut Universitaire du Cancer de Toulouse l’IUCT oncopole rassemblant une partie hospitalière IUCT et une partie recherche CRCT. Plusieurs oncopoles étaient prévus par le 1er plan cancer de 2003 et c’est en 2004 sur le site dévasté de l’usine ASF qu’a été construit cet oncopole avec des partenaires publics et privés. 1 miliard d’euros, 10.000 patients chaque année, 200 patriciens, 170 chercheurs. Et cette année c’est un essai toulousain le 2046 qui a fait la « une » à l’Asco. Bravo à l’équipe, au présentateur le docteur Damien Pouessel et à sa responsable, le professeur Elisabeth MOYAL.
Le levothyrox ou levothyroxine, présence inquiétante de la dextrothyroxine ?
Le levothyrox de Merck ou la levothyroxine, nom générique, est une substance pour stimuler une thyroïde sous-active. Une association de patients a demandé à un laboratoire étranger d’analyser le médicament. Résultats, sous-dosage de levothyroxine et présence d’un produit non signalé, la dextrothyroxine interdite aux Etats-Unis. Merck avait sur demande de l’ANSM, en mars 2017, modifié la composition car il y avait de grosses différences de dosage entre les lots et aussi remplacé le lactose mal supporté. Chaque comprimé sécable est à prendre chaque matin à jeun et comprend 25, 50 et même 200 micro-grammes pour le 25, le 50, ou le 200 d’une substance très difficile à peser pour le 25 micro-grammes et en plus très instable. Les thyroïdologues connaissaient bien le problème. La France est le 1er et seul pays d’Europe à tester la nouvelle formule. Pour la Ministre de la santé Il n'y a pas de fraude. Rien n’explique cependant la présence de la dextrothyroxine, une substance interdite aux États-Unis pour des effets secondaires similaires à ceux décrits aujourd'hui par les malades de la thyroïde, crampes, maux de tête, vertiges et perte de cheveux. On parle aussi de nanoparticules, de débris d’acier. La production est faite à Semoy dans le Loiret. Des perquisitions ont été faites chez Merck qui abandonnera cette nouvelle formule fin 2018. Plusieurs médicaments de substitution sont actuellement disponibles en France.
La traduction en français des 70 présentations à l’Asco 2018
Le congrès de l’oncologie mondiale a eu lieu à Chicago du vendredi 1er juin au mardi 5 juin. Les 70 présentations (10 sur les métastases et 60 sur les tumeurs de cerveau) ont été publiées, comme chaque année depuis 17 ans, sur le site de GFME, une semaine avant l’ouverture du congrès. La présentation qui a eu le plus de succès, la 2046 est un essai toulousain de phase 1 de durvalumab inhibiteur du point de contrôle PD-L1 avec une radiothérapie stéréotaxique hFSRT en 3 fractions de 8 Gy sur glioblastome récurrent avec 1 patient sur les 6 premiers à avoir une réponse complète.
Les premières présentations sont toujours les plus attendues, la 2000, allemande, concernait 2 vaccins peptidiques personnalisés (7 peptides), avec GM-CSF et Poly-ICLC sur glioblastome nouvellement diagnostiqué, GAPVAC-101, 16 patients. Les patients suivaient aussi le protocole classique. Après le 4ème cycle de temozolomide adjuvant 11 patients ont reçu un 2ème vaccin avec de nouveaux antigènes APVAC2. La survie sans progression 14,2 mois et la survie globale 29 mois. La 2ème présentation 2001, allemande aussi avec un vaccin peptidique ciblant la mutation IDHR132H, NOA-16, pour astrocytome nouvellement diagnostiqué de grade III et IV, toujours en plus du traitement standard. 29 patients ont reçu chacun 8 vaccins. 87% avaient une stabilité de la maladie.
La 2002 est américaine avec un inhibiteur AG-881 ciblant également la mutation IDH1/2 pour gliomes mIDH1-2 récurrent ou progressifs. 93 patients soignés, le dosage limite est de 100 mg. Les premières données non disponibles ont été présentées lors de la réunion. Comme toujours des présentations sur les métastases, 10, dont on commence à s’apercevoir qu’elles sont très sensibles aux inhibiteurs du point de contrôle.
La recherche française toujours très présente à l’Asco 2018
La recherche française a encore été très présente à l’Asco 2018 avec 6 présentations sur 70.
2004-Faisabilité et bénéfice de l'inscription moléculaire dans les essais de phase précoce pour les patients atteints de gliomes récurrents.
Gustave Roussy, Salpêtrière, ICO, Centre René Gauducheau, Foch, Suresnes, ICM, Paris.
Un sous-ensemble de patients atteints d'un gliome récurrent peut bénéficier de l'incorporation du génotypage tumoral pour guider leur inscription dans les EFC. L'accélération de l'utilisation de la génomique prospective pourrait augmenter le pourcentage de patients susceptibles de bénéficier de cette stratégie.
2005-Cibles exploitables impliquant des récepteurs du FGF dans les gliomes, spécificités moléculaires, distribution spatiale, résultat clinique et phénotype radiologique
Foch, Suresnes, Fondation Rothschild, Salpêtrière, IGCNO, Paris, Villejuif, ICM, Pierre et Marie Curie-Paris 6
Il s’agit de préciser les caractéristiques cliniques, moléculaires et radiologiques des gliomes diffus avec des fusions FGFR3-TACC3 ou des mutations FGFR1, qui sont toutes deux réalisables avec de nouveaux inhibiteurs anti-FGFR par voie orale.
Les gliomes avec des fusions de gènes FGFR3-TACC3 et des mutations de FGFR1 représentent deux entités spécifiques avec des caractéristiques anatomiques, cliniques et moléculaires distinctes. Ils devraient être reconnus parce que les deux modifications sont admissibles aux essais cliniques anti-FGFR en cours
2016-Le SonoCloud, données d'innocuité et d'efficacité d'une étude de phase I d'un dispositif implantable à ultrasons pulsés de faible intensité (LIPU) pour ouvrir la barrière hémato-encéphalique (BHE) de patients traités par chimiothérapie pour un glioblastome récurrent.
ICM, CarThera, Lyon, La Pitié-Salpêtrière.
27 patients ont été implantés avec des dispositifs LIPU et ont été traités par ultrasons. Le LIPU est bien toléré et augmente l'efficacité des traitements médicamenteux dans le cerveau.
2028- Paysage génomique du pinéoblastome.
Hôpital Wertheimer, CHU Lyon, CHU Nancy, Gustave Roussy, CHU St. Etienne.
Le pinéoblastome (PB) est une tumeur cérébrale pédiatrique rare mais agressive qui provient de la glande pinéale. Les taux de survie globaux sont estimés à 50-60%, avec des patients plus jeunes (<5 ans) s'en tirant beaucoup plus mal (15-40%). Les PB se divisent en quatre groupes, chacun avec un profil génétique et clinique distinct. Ces résultats auront des implications importantes pour la stratification précise des patients et formeront la base pour des études précliniques de thérapies basées sur la biologie.
2042- Prophylaxie secondaire avec le romiplostim pour la thrombocytopénie induite par le témozolomide chez les patients atteints d'un glioblastome nouvellement diagnostiqué.
Inserm, U-119 Lille, CHU Lille, Centre Oscar Lambret, Hôpital Pitié-Salpêtrière, Hospices Civils de Lyon, CHU Timone.
La thrombocytopénie est un événement indésirable majeur de la chimiothérapie par le temozolomide. Les agonistes des récepteurs de la thrombopoïétine, tels que le romiplostim, permettent d'assurer une exposition adéquate à la chimiothérapie chez les patients atteints de glioblastome et subissant une thrombocytopénie précoce et sévère induite par une chimiothérapie.
La recherche toulousaine qui a séduit tous les présents à l’ASCO et les télés
2046-Radiothérapie stéréotaxique hypofractionnée + l’anti-PD-L1 durvalumab dans le glioblastome récidivant, résultats de la phase I de l'essai STERIMGLI.
Damien Pouessel, Elizabeth Moyal, Hôpital Saint Louis, Paris, ICO - René Gauducheau, IUCT-Oncopole, Toulouse, Institut Claudius Regaud
Les études cliniques montrent des résultats encourageants lorsque les inhibiteurs du point de contrôle sont combinés avec la radiothérapie RT à haute dose. La combinaison de 3 fractions de 8 Gy de hFSRT avec 1500 mg de Durvalumab toutes les 4 semaines pour le glioblastome récurrent est bien tolérée et prometteuse avec 1 réponse complète sur les 6 premiers patients. Le Docteur Damien Pouessel a ensuite été très sollicité par les télévisions américaines qui ne connaissaient pas Toulouse mais AIRBUS-City.
On retrouve facilement le lien pour la vidéo sur le site, Asco et aller sur lire de la 2046 ou cliquer ici.
Actualité 657 du 8 avril 2018
La signalisation réciproque entre les cellules souches de glioblastome et les cellules tumorales différenciées favorise la progression maligne
Ce sont plusieurs grandes équipes américaines qui s’intéressent à la diaphonie entre les cellules souches de glioblastome (CSG) et leur niche de soutien pour leur développement. Les équipes ont étudié la signalisation réciproque entre les CSG et leur progéniture différenciée de cellules de glioblastome (DGC) et ont constaté que les DGC accéléraient la croissance tumorale des cellules souches GSC. Les DGC exprimaient préférentiellement le facteur neurotrophique dérivé du cerveau (BDNF), alors que les GSC exprimaient le récepteur NTRK2 du BDNF et une expression augmentée de BDNF des CSG accroit la croissance tumorale des DGC. Pour déterminer les médiateurs moléculaires de cette signalisation paracrine BDNF-NTRK2, les équipes ont exploré les profils transcriptionnels et épigénétiques des GSC et DGC révélant l'expression préférentielle de VGF par les GSCs. Le facteur de croissance vasculaire VGF joue un double rôle dans la hiérarchie du glioblastome en promouvant la survie des cellules souches GSC in vitro et in vivo tout en soutenant également la survie des DGC en induisant la sécrétion de BDNF dans les DGC. Collectivement, ces données démontrent que les cellules de glioblastome différenciées coopèrent avec des cellules tumorales de type souche via la signalisation paracrine BDNF-NTRK2-VGF pour favoriser la croissance tumorale.
Pubmed : 29625067
Actualité 658 du 14 avril 2018
Deux inhibiteurs concomitants BRAF/MEK (dabrafenib et trametinib) efficaces sur des tumeurs cérébrales primaires de haut grade avec la mutation BRAF V600
Deux inhibiteurs concomitants BRAF/MEK (dabrafenib et trametinib) efficaces sur des tumeurs cérébrales primaires de haut grade avec la mutation BRAF V600. C’est le grand centre américain Johns Hopkins de Baltimore qui teste des inhibiteurs BRAF/MEK sur le glioblastome. Des mutations BRAF V600 ont été identifiées chez les patients avec des tumeurs cérébrales primaires plus fréquemment depuis que les tests moléculaires sont largement disponibles. Un traitement ciblé avec des inhibiteurs de BRAF a été tenté sur des cas individuels avec certaines réponses, tandis que d'autres n'ont montré aucune réponse ou développé une résistance. Le travail préclinique suggère que les gliomes pourraient être plus sensibles à l'utilisation simultanée de l'inhibition de BRAF et MEK pour la suppression de la voie MAP kinase. 1 patient avec glioblastome a continué d'avoir une maladie stable après 16 mois de traitement, un cas encourageant mais un travail supplémentaire est nécessaire pour comprendre les taux de réponse, la durée et la survie dans les tumeurs cérébrales primaires.
Pubmed : 29632053
Actualité 659 24 avril 2018
Etude multicentrique de phase IB de l'orotate de carboxyamidotriazole et du témozolomide pour glioblastome récurrent et nouvellement diagnostiqué et d'autres gliomes anaplasiques
Un travail mixte américano-Suisse avec Memorial Sloan Kettering qui s’intéresse à L'orotate de carboxyamidotriazole (CTO), un nouvel inhibiteur oral des canaux calciques non voltage-dépendants avec des effets modulateurs dans plusieurs voies de signalisation cellulaire et des effets synergiques avec le temozolomide dans les modèles de glioblastome.
2 cohortes.
-cohorte 1, patients avec gliome anaplasique récurrent ou glioblastome qui ont reçu des doses croissantes de CTO (219 à 812,5 mg)/m2 une fois par jour ou 600 mg dose fixe une fois par jour) en combinaison avec le temozolomide (150 mg/m2, 5/28 jours).
-cohorte 2, patients avec glioblastome nouvellement diagnostiqué, doses croissantes de CTO (219 à 481 mg/m2 /une fois par jour) + radiothérapie + temozolomide 75 mg/m 2, suivis de temozolomide 150 mg à 200 mg/m2, 5/28 jours. 47 patients inclus avec traitement bien toléré. Les toxicités comprenaient la fatigue, la constipation, la nausée et l'hypophosphatémie. La pharmacocinétique a montré que CTO n'a pas modifié les niveaux de temozolomide et les concentrations thérapeutiques ont été atteintes dans les tumeurs de cerveau. Aucune toxicité limitant la dose n'a été observée.
La dose de phase II recommandée était de 600 mg/jour.
Dans la cohorte 1 de 27 patients, 1 réponse complète et 6 réponses partielles, y compris avec MGMT non méthylé ou chez des tumeurs ayant échappé au bevacizumab.
Dans la cohorte 2 de 15 patients avec glioblastome nouvellement diagnostiqué, survie sans progression de 15 mois et survie globale non atteinte (suivi médian de 28 mois, survie globale > 2 ans de 62%. Le séquençage des gènes a révélé un taux élevé de réponses parmi les tumeurs avec EGFR++, par des mécanismes de résistance acquise impliquant des mutations dans les gènes de réparation et/ou les composants en aval TSC2, NF1, NF2, PTEN et PIK3CA. CTO peut être combiné en toute sécurité au temozolomide ou à la radiochimiothérapie dans les gliomes anaplasiques et les glioblastomes, montrant une pénétration cérébrale favorable et des signaux prometteurs d'activité dans cette population difficile à traiter.
Pubmed : 29683790
Actualité 660 24 avril 2018
La forme mutée d'IDH1 favorise la formation de gliome in vivo
Ce sont plusieurs équipes américaines de Salt Lake City dans l’Utah qui s’intéresse à la mutation IDH1 dont on ne connait pas très précisément le rôle. Le gène IDH1 (isocitrate déshydrogénase) est un gène fréquemment muté dans les gliomes de bas grade et dans les glioblatomes secondaires. Un rôle causal de la mutation IDH1 R132H dans la gliomagenèse a été proposé, mais n’a jamais été prouvé. Les chercheurs ont évalué le rôle d’IDH1 R132H dans le développement du gliome par altérations génétiques pertinentes in vitro et in vivo. Les astrocytes exprimant IDH1 R132H présentaient des taux élevés de 2HG, avec une augmentation de la prolifération. Bien que non suffisant en soi, IDH1 R132H a coopéré avec PDGFA et la perte de Cdkn2a, Atrx et Pten pour promouvoir le développement du gliome in vivo. Ces tumeurs ont un fonctionnement, un profil génétique et histologique comparable au glioblastome secondaire proneural avec mutation IDH1. Ces résultats soutiennent l'hypothèse que la mutation IDH1 R132H favorise le développement du gliome.
Pubmed : 29719265
Actualité 661 18 juin 2018
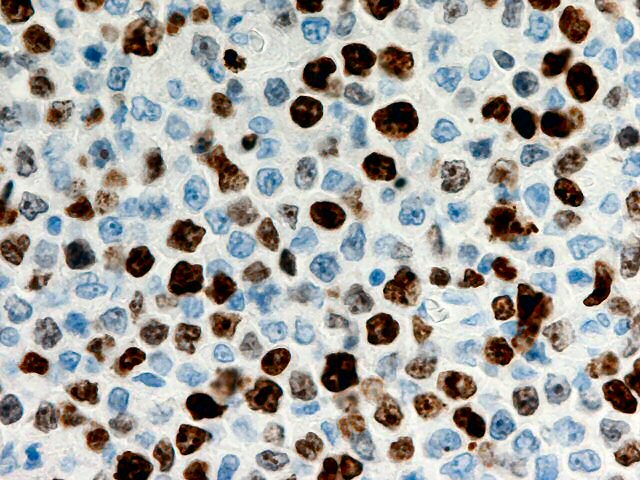
Evaluation du marqueur de prolifération KI-67 dans les gliomes, variabilité inter-observateurs et quantification numérique
C’est l’image d’un glioblastome, le KI-67 est le rapport des cellules sombres sur le total des cellules. Les indices MIB1 et KI-67 sont généralement mesurés en comptant les cellules dans la région « point chaud » très proliférative et sur la moyenne de l’échantillon. KI-67 est plus faible que MIB1 car il évalue la fraction de cellules tumorales entrées en cycle cellulaire, G1, S, G2, M, mais qui ne se diviseront pas forcément alors que MIB1 évalue le nombre de cellules effectivement capables de se diviser. KI-67 est aussi plus complexe à mesurer que MIB1 mais peut se faire sur des échantillons de petite taille. Ce sont plusieurs équipes danoises qui s’intéressent à la précision de l’index de prolifération KI-67 et qui constate qu’il y a des divergences entre le comptage manuel de différents observateurs (points chauds et moyennes) ou avec des logiciels numériques de comptage. L’objectif était d'évaluer la variabilité du KI-67 LI entre deux pathologistes A et B et entre les pathologistes A ou B et la quantification digitale. Dans des échantillons de 235 gliomes de bas et de haut grade, deux pathologistes (A et B) ont estimé le KI-67 LI sur des lames tumorales. Un logiciel conçu pour identifier les noyaux positifs et négatifs selon la couleur a aussi calculé le KI-67 LI. Les proportions d'accord entre les observateurs et l'analyse digitale pour KI-67 LI étaient :
Entre les 2 observateurs A et B et entre observateurs A et B contre analyse digitale numérique C
-A / B: 46% (κ = 0,32), 54% désaccord
-A / C: 37% (K = 0,26) 63% désaccord
-B / C: 37% (K = 0,26). 63% désaccord
La variabilité inter-observateurs était importante entre les pathologistes et les analyses numériques. La quantification numérique de KI-67 LI dans les gliomes est faisable, mais la bonne valeur entre laboratoires doit encore être améliorée. Les deux méthodes sont complémentaires et leurs significations différentes. La communication du KI-67 à des bas grades les inquiètent plus qu’elle ne les informe. L’étude 2030 de l’ASCO cette année porte sur la différentiation grade 1 ou 2 des méningiomes par MIB1
Pubmed : 29885671
Mais qui est donc Claudius Regaud ?
Claudius Regaud (30/01/1870 à Lyon-29/12/1940 à Couzon-au-Mont-d'Or en banlieue lyonnaise) était un médecin français, biologiste, l'un des pionniers de la radiothérapie à l'Institut Curie. S’appuyant sur le fait que l’exposition aux rayons X des testicules rendait les gens stériles, il avait découvert que la radiothérapie détruisait les cellules qui se divisaient rapidement, celles des cancers comme celles des gamètes. En 1914, il dirige le Pavillon Pasteur de l'Institut du Radium. Il est l’homologue de Marie Curie. Il est envoyé au front comme médecin. Il occupe ensuite différentes fonctions et est considéré comme le fondateur de l’institut Curie
Les derniers essais en cours d’après le site Clinicaltrials
1- (09/2017), phase 2, Dana Farber Etats-Unis, bavituximab + temozolomide + radiothérapie pour glioblastome nouvellement diagnostiqué.
Le bavituximab de Peregrine est un anticorps monoclonal immunomodulateur expérimental qui cible la phosphatidylsérine (PS), un phospholipide qui inhibe la capacité des cellules immunitaires à reconnaître les cellules tumorales.
2- (06/2018), France Lille, phase 1b, TG02 + temozolomide (MGMT méthylé) ou radiothérapie (MGMT non méthylé) pour astrocytome III nouvellement diagnostiqué ou récidivant chez patients âgés IDH1R132H non muté.
TG02 est un nouvel inhibiteur oral de multiples kinases cycline dépendantes, CDKs, JAK2 et FLT3
3 - (06/2018), France, La Timone et Clairval, Cohorte prospective de patients atteints de glioblastome nouvellement diagnostiqué, analyse de MMP2 et MMP9 et corrélation avec les images IRM.
MMP2 et MMP9 dégradent le collagène des cellules.
4 - (07/2018), Etats-Unis, phase 1, Ibrutinib + radiothérapie + temozolomide chez des patients atteints d'un glioblastome nouvellement diagnostiqué
L'Ibrutinib (Imbruvica) est une petite molécule qui se lie à la tyrosine kinase de Bruton (BTK) importante chez les lymphocytes B. Le médicament est déjà utilisé dans les lymphomes ou la leucémie.
5 - (06/2018), Phase 1, Etats-Unis, Washington, 4 vaccins peptidiques Neovax en sous-cutané + anti-PD1, Nivolumab (Opdivo) seul puis + Ipilimumab (Yervoy) pour glioblastome nouvellement diagnostiqué, MGMT non méthylé.
Neovax ce sont 4 vaccins poly-ICLC injectés en sous-cutané chaque semaine.
7 - (03/2018), Etats-Unis, Lee Moffitt, Tampa, Floride, phase 1, Pembrolizumab (Keytruda) + Vorinostat (Zolinza) + temozolomide + radiothérapie pour glioblastome nouvellement diagnostiqué.
Vorinostat est un inhibiteur d’histone déacétylase HDAC.
8 - (06/2018), Etats-Unis, Clinique Cleveland, phase 1, ruxolitinib + radiothérapie + temozolomide sur gliomes III et glioblastome.
le ruxolitinib est un inhibiteur des kinase Janus, JAK 1 et 2
9 - (07/2018), Etats-Unis, MD Anderson, phase 1, EDO-S101 pour glioblastome MGMT non méthylé
La tinostamustine (EDO-S101) améliore l'accès aux brins d'ADN dans les cellules cancéreuses et réduit la résistance de MGMT non méthylé qui récupère les CH3 des chimiothérapies alkylantes.
Ils nous ont quittés
-Le 15/06/2018, Anne-Marie, 59 ans, la femme de Gilles.
Adhésion, sites Internet
Les adhésions ont baissé, 13 seulement cette année contre 23 l’année dernière. Le site Internet de GFME possède 5 emplacements
Sites sécurisés : https://glioblastome.fr et https://gfme.fr
Sites non sécurisés :
gfme.free.fr
gfme.fr
glioblastome.net
Nous somme 3ème chez Google et 3ème et 10ème chez Bing en affichage sur saisie du mot "glioblastome".
Mailing-listes et Facebook
GFME c’est aussi 2 mailing-listes, l’une pour les grades IV de 428 membres et l’autre des gliomes de bas grade, ou anaplasiques III, de 275 membres, soit 703 membres au total contre 682 l’année précédente. Le nombre de messages est en forte baisse avec 349 messages cette année contre 1070 l’année précédente sur la 1ère liste et 58 cette année contre 102 l’année dernière sur la 2ème liste.
La page Facebook est très visitée.
Rendez-vous pour le prochain numéro, le n° 50 en Octobre 2018
Glioblastome Association
Michèle Esnault (GFME)
Bât A, boîte 4
22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 €/Renouvellement 7,5 €.
Reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N
Michèle Esnault Fondatrice de GFME en 2001 (16 ans)