21/05/2022
GFME, les espoirs, vaccins
Suite

Immunothéravie PD1-PD - L1 et vaccin polio surprenants sur le glioblastome
Une vidéo à découvrir sur l'immunothérapie + vaccin virus oncolytique, le duo gagnant *****
Dernières nouvelles de la recherche par IBTA de Févier 2019 cliquer ici
Des cellules souches utilisées pour surmonter la résistance du glioblastome à l'immunothérapie par inhibiteurs PD1 ou PD-L1 efficaces lors d'expérimentations animales
Un rapport publié dans la revue Nature Communications a décrit une technique utilisant des cellules souches pour inverser la résistance des tumeurs cérébrales au blocage du point de contrôle PD-1, un type d'immunothérapie. Dans une série d'expériences sur des animaux, des cellules souches isolées de la moelle osseuse ont été utilisées pour reprogrammer les tumeurs du glioblastome afin de les rendre sensibles à l'immunothérapie. Une étude récente de phase 3 n'a pas démontré de bénéfice en termes de survie avec la monothérapie PD-1 contre le glioblastome récurrent, et cette nouvelle approche pourrait contribuer à rendre ce traitement plus efficace. Lire la suite
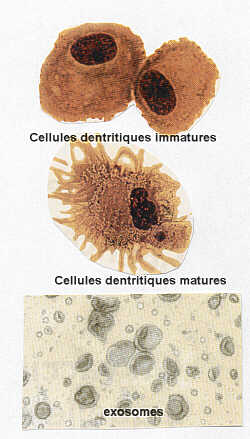
Cellules dendritiques et exosomes

L'immunothérapie avec le nivolumab est actuellement en essai sur les glioblastomes nouvellemnt diagnostiqués dans 8 CHU en France
Les dernières nouvelles sur les vaccins anti PD1-PD-L1
Celgene travaille avec BeiGene pour développer son inhibiteur de PD-1, BGB-A317, pour traiter des tumeurs solides.
18 JUILLET 2017
Voir plus
Opdivo (nivolumab) étend la survie, a moins d'impact sur la vie chez les patients atteints de cancer de la tête et du cou que la chimie standard, des spectacles d'étude.
19 JUILLET 2017
Voir plus
NT-219 resensibilise le cancer au Keytruda (pembrolizumab), interrompt la progression de la tumeur, montre l'étude.
20 JUILLET 2017
Voir plus
Opdivo, Yervoy et Keytruda (pembrolizumab), peuvent produire des réactions défavorables rares affectant l'oeil, selon la FDA.
21 JUILLET 2017
Voir plus
Les nouveaux vaccins en test sur les glioblastomes, la cible prometteuse PD1/PD-L1
Aujourd’hui, après l’échec des vaccins dendritiques et peptidiques totalement inefficaces, une nouvelle génération de vaccins inhibiteurs de PD1 semble promise à un bel avenir. Il s'agit de bloquer les voies par laquelle la tumeur endort le système immunitaire, PD1/PD-L1 ou CTLA-4 (Lymphocyte cytotoxique antigène 4). L’antigène 4 des lymphocytes T cytotoxiques (CTLA-4) est un régulateur négatif de l’activation des cellules T. Ipilimumab (Yervoy-MDX010-20)
Ipilimumab est un inhibiteur de CTLA-4, qui conduit à une activation des cellules T, à leur prolifération, et l’infiltration des tumeurs par les lymphocytes, aboutissant à la mort des cellules tumorales. Son mécanisme d’action est indirect, en activant la réponse immunitaire via les lymphocytes T.
Nivolumab (BMS-936558; MDX-1106) de BMS
Le nivolumab en échec dans un essai de phase III
BMS annonce le 4/4/2017 que l'essai de phase III visant à remplacer Avastin par le nivolumab à la récidive des glioblastome, traitement validé par la FDA mais pas par l'Europe est un échec.
Plusieurs essais sont toujours en cours après Checkmate-143 qui est un échec, il y a Checkmate-498 et Checkmate-548 qui étudie le Nivolumab avec d'autres traitements comme la radiothérapie , le Temodal ou le bevacizumab (Avastin).
Le nivolumab est un anticorps monoclonal inhibiteur de PD1. Essai en 12/2014 de temozolomide en combinaison avec ipilimumab et/ou nivolumab + radiothérapie pour glioblastome nouvellement diagnostiqué.
MEDI4736
Essai de phase II, 12/2014, Etats-Unis et Australie, MEDI4736 d’Astra Zeneca pour glioblastome nouveau ou récurrent, avec ou sans bevacizumab ou radiothérapie, 3 bras.
Le pembrolizumab ou Keytruda ou MK-3475 de Merkx.
Médicament immunothérapeutique, inhibiteur de PD1 qui augmente la mort des cellules tumorales par activation des lymphocytes T cytotoxiques endormis par la tumeur en essai de phase II, 01/2015, au Dana Farber, avec bevacizumab pour glioblastome récurrent et en phase II aussi, 01/2015, au MD Anderson avant et après chirurgie.
L'immunothérapie, la révolution anticancer
Le Parisien titrait récemment sur sa une : « Cancer : enfin un progrès décisif ». Il se confirme, en effet, que l’immunothérapie va désormais jouer une place importante et ce qui est totalement nouveau, c’est qu’elle va permette des traitements efficaces contre des cancers très agressifs, pour lesquels on ne disposait que de peu de solutions. On n’a jamais observé de tels résultats.
Ne pas prendre d'antibiotiques pendant l'immunothérapie
Les antibiotiques affectent l’efficacité d’un traitement du cancer par immunothérapie, selon une étude française publiée dans la revue Science. Or, environ 20 % des malades du cancer sont sous antibiothérapie, indiquent les chercheurs.
L’immunothérapie a prouvé sa supériorité sur le traitement standard dans la prise en charge du mélanome métastatique, du cancer du poumon, du rein ou encore de la vessie mais son efficacité est limitée à une proportion de malades », rapportent les chercheurs. « Nos travaux expliquent en partie pourquoi certains patients ne répondent pas ». « Les immunothérapies, par transfert de lymphocytes T activés ou par anticorpsmonoclonaux (anti-CTLA4 ou anti-PD1) ou bispécifiques, visent à déclencher l'activation du système immunitaire du patient », précise le communiqué de l'Inserm. Ces travaux ont été menés par le Dr Bertrand Routy et la Pr Laurence Zitvogel avec leurs collègues de Gustave Roussy, l’Inserm, l’Inra, l’AP-HP, IHU Méditerranée Infection et l’Université Paris-Sud. Dans une première étude, menée avec 249 patients traités par immunothérapie basée sur l’anti-PD-1/PD-L1 pour un cancer avancé du poumon, du rein ou de la vessie, 28 % avaient pris des antibiotiques à cause d’une infection dentaire, urinaire ou pulmonaire. En créant un déséquilibre du microbiote intestinal (ou dysbiose), les antibiotiques pris deux mois avant et jusqu’à un mois après le début du traitement a eu un impact négatif sur la survie sans progression de la maladie et la survie globale dans ces trois cancers.
Source
Une découverte
importante
Dans
les années 1880, des médecins avaient déjà
constaté que des tumeurs dont sont atteints des patients qui contractaient
des maladies infectieuses régressent parfois. Tout se passait comme si
le système immunitaire stimulé par l'infection devenait plus efficace sur les tumeurs et c'est ainsi que naquit l'immunité antitumorale,
la lutte contre les tumeurs en utilisant les défenses de l'organisme. Malgré
quelques succès d'immunothérapie, les résultats n'ont guère
été, jusqu'à ce jour, probants.
L’association de souches virales avec l’immunothérapie ouvre des perspectives nouvelles contre le cancer
L’utilisation de virus oncolytiques pourrait bientôt devenir une arme incontournable contre le cancer. Cette stratégie thérapeutique est en train de monter en puissance avec des travaux dans différents laboratoires et grâce à l’arrivée de l’immunothérapie. C’est ce que montrent plusieurs études récentes. L’idée d’utiliser des virus dits «oncolytiques» remonte à de nombreuses années. Dès 1924, des chercheurs américains observent que certains patients atteints d’un cancer voient leur tumeur régresser après une infection virale. Ils en concluent que des virus peuvent infecter spécifiquement des cellules tumorales et les détruire. Des virus atténués utilisés comme vaccins sont alors développés dans ce but et un premier virus oncolytique issu d’une souche d’herpès obtient une autorisation de mise sur le marché contre le mélanome aux États-Unis en 2015 (le T-vec). D’autres sont en cours d’essai aux Etats-Unis sur le glioblastome avec un vaccin contre le virus atténué de la polio qui semble pour cette maladie, le virus idéal.
Certains de ces virus pénètrent naturellement dans les cellules malades, d’autres doivent être transformés comme les virus dérivés de la rougeole, de l’herpès ou de la variole. Il suffit ensuite de les injecter au niveau de la tumeur pour qu’ils effectuent leur travail», détaille-t-il. Mais alors que les promesses de cette stratégie thérapeutique étaient réelles, elles deviennent immenses avec l’arrivée des traitements d’immunothérapie.
Une explication s’impose. Les scientifiques ont découvert que le système immunitaire était verrouillé chez les patients atteints de cancer. La tumeur endort le système immunitaire et parvient à bloquer l’activité des lymphocytes T contre elle-même de sorte que l’organisme tolère des cellules malades alors qu’il devrait normalement les éliminer. C’est ce qui permet aux tumeurs de croître en échappant à la surveillance immunitaire. La découverte de ce mécanisme d'échappement, la lialison PD1 du lymphocyte avec son ligand PD-L1 sur la cellule tumorale doit être ihibé. Plusieurs médicaments sont en esai actuellement sur le glioblastome, des inhibiteurs de PD-L1 comme le Pembrolizumab.
Le blocage de PD1 - PD-L1 n'est pas
suffisant
La tumeur parvient aussi à échapper au système immunitaire en se cachant comme les enfants. Pour la rendre visible, on a eu l'idée d'utiliser les vaccins contre les virus atténués et pour le glioblastome c'est le virus de la polio qui fait peur. Alors les essais se poursuivent actuellement mais les premiers résultats sont exceptionnels.
Seulement, comme le rappellent les auteurs d’une nouvelle étude parue dans Science Translational Medicine, ces traitements fonctionnent seulement si les cellules T sont là, inactives mais bien présentes. Et c’est là que le virus oncolytique entre en scène. Ces chercheurs montrent qu’en provoquant la libération de débris cellulaires tumoraux après avoir infecté et détruit des cellules cancéreuses, le virus envoie des signaux de danger au système immunitaire qui se met à produire des nouveaux lymphocytes T anticancéreux. Leur virus en question (PVSRIPO, un mélange de poliovirus et de rhinovirus) est d’ailleurs en cours de développement contre les gliomes avancés. Ils ajoutent à cela un traitement d’immunothérapie qui favorise et libère l’activité toxique de ces cellules T au niveau de la tumeur. Celle-ci se retrouve attaquée de toutes parts. C’est ce que viennent de confirmer des résultats d’essais cliniques parus dans la revue Cell. Des patients atteints de mélanome ont reçu une association de virus oncolytique T-vec et d’anti-PD1 (immunothérapie). Deux tiers des patients ont vu leur tumeur régresser et pour un tiers d’entre eux, l’élimination a été totale. «Des résultats tout simplement impressionnants», conclut Marc Grégoire.
Un
succès sur le mélanome relance la méthode
C'est
un essai très encourageant de vaccination contre une forme de cancer de la peau,
le mélanome, qui vient d'être réalisé. Cet essai qui a porté sur 25 patients a entraîné une régression des métastases chez cinq d'entre eux et une rémission
totale chez deux patients traités depuis plus de trois ans, a annoncé Aventis
Pasteur, promoteur de cet essai. Un temps éclipsée par les promesses de la
génétique, la stratégie des "vaccins anti-cancer" est de nouveau d'une
grande actualité et les plus gros laboratoires semblent aujourd'hui décidés à
s'y investir.
Des
antigènes de tumeur reconnus
Depuis
plusieurs années, les cancérologues ont appris que dans de nombreuses formes de
cancers, les cellules des tumeurs portent à leur surface des antigènes qui peuvent être reconnus par les cellules de protection du système immunitaire, les lymphocytes T, qui sont capables de les détruire. La poursuite de ces
essais permettra véritablement de déterminer si, par ce procédé, on peut déclencher
une réponse immunitaire telle, qu'elle est capable d'éliminer les cellules cancéreuses.
Comment
ça marche ?
On effectue une prise de sang puis on sélectionne une variété
de globule blanc, les cellules dentritiques immatures qui mises en contact
avec l'antigène tumoral et avec l'aide de facteurs de croissance spécifiques
vont se différencier.
On retient les exosomes
Ce ne sont pas les cellules
dentritiques qui seront réintroduites chez le patient mais en sous-cutanée,
des petites cellules sécrétées par ces cellules dentritiques,
les exosomes, riches en molécules du complexe majeur d'histocompatibilité.
Des essais concluants sur l'animal
Dans un essai sur des souris, 60% ont
rejeté la tumeur. Ce traitement par les exosomes est beaucoup plus efficace
que par l'introduction des cellules dentritiques. De plus les souris ayant rejeté
la tumeur ont acquis une "mémoire" et rejettent toute tumeur identique qu'on essaie de réimplanter.
Un nouveau vaccin dendritique ICT-107 intéressant sur les glioblastomes qui vise les cellules souches tumorales
GFME 26/01/2010 n° 288
Retrouver l'article original
Nouvel essai thérapeutique d'ImmunoCellular avec un vaccin ICT-107 qui cible les cellules souches tumorales pour lutter contre les récidives.
LOS ANGELES, ImmunoCellular publie aujourd'hui les résultats d'un essai clinique dans lequel il a été montré que certains antigènes spécifiques sont très exprimés sur les cellules souches tumorales (CSCs). Cela suggère que le vaccin d'IMUC, ICT-107 qui vise les antigènes de ces cellules souches peut aussi viser efficacement les autres cellules tumorales et éviter les récidives.
Les cellules souches CSCs utilisées dans l'étude d'IMUC ont été isolées des tumeurs retirées à la chirurgie de cinq malades avec glioblastome, le type le plus courant et les plus agressif des tumeurs de cerveau. Ces CSCs ont été trouvées pour avoir de plus hautes expressions de 3 antigènes visé par ICT-107—Her-2/neu, AIM2, et TRP-2—dans les cellules qui composent la tumeur. “ICT-107 peut soutenir le système immunitaire à combattre les cellules souches tumorales, en plus des cellules qui composent le reste de la tumeur ” a précisé le Dr. John Yu, MD, Président de IMUC, “Nous croyons que la capacité de viser les cellules souches tumorales est critique pour prévenir les récidives de la maladie.”
Le Dr. Manish Singh, Président et PDG d'IMUC, a ajouté, “les cellules souches tumorales sont comme les racines des mauvaises herbes et peuvent être indétectables après que la tumeur ait été retirée et si elles ne sont pas visées efficacement, la tumeur reviendra surement. Nous croyons à la capacité de ICT-107 de viser de façon significative les cellules souche tumorales à la différence d'autres vaccins contre le cancer en développement.”
Dans un essai récent de phase I de ICT-107, les malades avec glioblastome récemment diagnostiqués qui ont reçu le vaccin ont démontré une augmentation à 12 mois dans la survie sans progression (PFS) après chirurgie. Cette survie se compare favorablement avec le PFS médian historique de 6,9 mois observé avec le traitement standard de chirurgie, radiothérapie et chimiothérapie de Temodal. 7/16 malades qui ont participé à l'essai continuent à survivre sans progression de la maladie après plus de 2 ans.
ICT-107 est vaccin dendritique qui agit en activant le système immunitaire d'un malade contre des antigènes tumeur-associés spécifiques. Cela est possible en extrayant les cellules dendritiques d'un malade, en les chargeant avec les antigènes, et en les réintroduisant dans le corps du malade pour déclencher une réponse immunisée.
Les 6 antigènes tumeur-associés utilisés dans le vaccin ICT-107 sont AIM2, Ses 2/neu, gp-100, MAGE-1, TRP-2 et IL13Ra2. Ces antigènes sont très exprimés dans le glioblastome ainsi que dans un grand nombre de cancers, y compris le cancer du sein, du pancréas, du côlon et le mélanome. ICT-107 peut, par conséquent, être utilisé sur des cancers multiples.
L'essai de phase II ouvert en 2011 est en cours.
mAb 425 (injection intra-tumorale)
Auteurs : P. Wersäll, je. Ohlsson, P. Biberfeld, V. P. Collins, von S. Krusenstjerna, S. Larsson, H. Mellstedt et J. Boethius
Départements d'Oncologie,de neurochirurgie, de médecine nucléaire, Hôpital Karolinska, S-17176 Stockholm, et département d'Oncologie Expérimentale, Université Uppsala, Uppsala, Suède.
Les glioblastomes malins surexpriment souvent EGFR contrairement aux cellules normales du cerveau qui l'expriment peu. Un anticorps monoclonal de souris (IgG2A) (mAb 425) (EMD55900) (Merck KGaA, Bernstadt, Allemagne) visant EGFR a été expérimenté sur 8 malades avec glioblastome primaire ou périodique EGFR+. mAb a été injecté deux fois par semaine en intratumoral à l'aide d'une sonde implantable. Le dosage administré a varié de 4 mg à 120 mg. Chez 3 malades, une nécrose de la tumeur importante a été constatée avec infiltration des macrophages, les granulocytes et les cellules T. 3 malades supplémentaires ont développé des signes cliniques et radiologiques d'une réaction intense, locale. Les plus hautes doses ont paru provoquer une réaction plus prononcée. Cet anticorps mAb 425, anti EGFR peut induire une réaction intense, et une nécrose considérable dans le glioblastome. Cependant, le programme n'a pas pu être poursuivi, même après ajustement du dosage en raison des réactions sévères sur les tumeurs non retirées par chirurgie.
Autres vaccins
Rindopepinut (CDX 110) :
Celldex Therapeutics annonce le 4 janvier 2012 avoir commencé un essai de phase II de Rindopepimut (CDX 110) en combinaison avec Avastin (Bevacizumab) chez les malades avec le récepteur du facteur de croissance épidermique EGFR muté positif, EGFRvIII fréquent dans les glioblastome. Cette nouvelle étude s'ajoute à l'essai de phase III de Celldex + radiochimiothérapie de Temodal (Stupp) pour les malades avec glioblastome et EGFRvIII+ récemment diagnostiqués.
L'essai de phase III pour glioblastome nouvellement diagnostiqué, commencé en novembre 2011, recrute toujours.
Un second essai avec EGFRvIII est en cours
APG 101 :
Le laboratoire allemand Apogenix a annoncé le relèvement de fonds supplémentaires pour accélérer l'essai clinique de Phase II de son médicament APG101 pour traiter le glioblastome GBM. Les résultats définitifs de l'essai sont attendus dans le premier quart de cette année. Un des investisseurs est le Centre de Recherche du Cancer allemand.
IMA950 au Royaume-Uni
IMA950 est un nouveau vaccin multi-peptide. Un essai de phase I a lieu depuis 2010 mais ne recrute plus pour glioblastome nouvellement diagnostiqué en plus du traitement standard de radio-chimiothérapie de Temodal. On ajoute aussi du GM-CSF pour augmenter les leucocytes.
Un autre essai de phase I avec Cyclophosphamide pour glioblastome, sans précision de nouveau ou récurrent recrute.
Autres vaccins avec virus ou vaccins dendritiques avec lysate de tumeur du malade
-IL13-PE38QQR (livraison intratumorale)
-Delta-24-RGD4C (en intra-veineuse, virus du rhume, désactivé qui vise surtout les cellules ayant perdu P53 ou la forme mutée de P53, +6 mois de survie)
-DCVax cerveau (injection intramusculaire de ce vaccin dendritique qui nécessite la chirurgie de la tumeur)
Un article très intéressant du magazine Rose qui informe sur l'immunothérapie des cancers