Glioblastome Association Michèle Esnault (GFME) Bât A, boite 4, 22 bd C. Flammarion 13001 Marseille
Voir le numéro 16 précédent
Voir le n° 18 suivant
Télécharger le journal en pdf

Patrick, un jeune niçois qui s'est battu avec rage
Le mot du président
J’adresse à chacun d’entre vous mes meilleurs vœux de bonne et heureuse année 2010. Je remercie chaleureusement tous les adhérents de GFME qui soutiennent et souvent de façon très généreuse son action mais aussi les 547 adhérents des 2 mailing-listes qui trouvent par ce moyen un espace de solidarité face à la maladie, et tous ceux qui fréquentent le site didactique de GFME reconnu par les professionnels de santé. Nous allons continuer notre action car je reste persuadé que la victoire est à portée. Ce numéro fait une large part au récepteur EGFR qui est le récepteur clé dans la prolifération des glioblastomes et pour lesquels tous les résultats des essais cliniques à ce jour ont été décevants. Mais nous sommes peut-être à l’aube d’une ère thérapeutique nouvelle. Avec des moyens très modernes, des équipes très performantes essaient aujourd’hui avec l’analyse micro array de vérifier les modifications génétiques mises en œuvre par la tumeur pour échapper aux traitements qui visent à bloquer les chemins de signalisation de la croissance tumorale et principalement la voie EGFR. On le sait depuis longtemps un traitement est très efficace au début, puis son efficacité diminue et cesse. Ce n’est pas la faute au médicament mais c’est la tumeur qui réussi à activer d’autres voies de signalisation pour assurer sa croissance. On le voit avec Avastin qui bloque efficacement la voie de la croissance vasculaire VEGF, le traitement est très efficace au début, dès les premiers jours, puis après quelques semaines, l’efficacité baisse. Le blocage de la voie de contournement, si elle est bien identifiée, est alors nécessaire. La tumeur peut encore utiliser d’autres voies de secours. On compare favorablement les voies de signalisation de la croissance tumorale au plan du métro parisien avec plusieurs itinéraires possibles pour aller d’un point à un autre. Viser la voie du remplaçant et celle principale du récepteur, donnera inévitablement une réponse plus longue à chaque traitement.
Les scientifiques découvrent comment les tumeurs échappent aux médicaments anti-EGFR
Des chercheurs au Ludwig Institut pour la Recherche sur le cancer (LICR) de Californie, et Moores, un centre anti-cancer UCSD viennent de découvrir comment les gliomes, arrivent à éviter les médicaments qui bloquent une protéine de signalisation cellulaire clé, le récepteur du facteur de croissance épidermique (EGFR), qui joue un rôle crucial dans la croissance tumorale. Ils ont découvert qu'une mutation particulière de EGFR (EGFRvIII) était importante non seulement pour initier la tumeur, mais pour sa croissance soutenue ou son maintien. L’étude parait le 18/01/2010 dans une édition en ligne des Débats de l'Académie Nationale de Sciences Américaines et ouvre de nouvelles perspectives. Les chercheurs précisent que si l'expression d'EGFR est nécessaire pour que les tumeurs continuent leur croissance, ils démontrent pour la première fois qu'il y a des mécanismes que la tumeur utilise pour contourner la nécessité de ce récepteur EGFR. Dans les gliomes malins agressifs, des copies supplémentaires du gène EGFR sont produites, et la moitié de ces tumeurs peuvent avoir un EGFR muté qui provoque la croissance de la tumeur et annonce un pronostic pauvre. Les essais cliniques avec des médicaments anti-EGFR ont été décevants. Les tumeurs de cerveau peuvent répondre au traitement dans un premier temps, mais ensuite, elles deviennent résistantes. L’équipe a voulu savoir si la mutation d'EGFR avait été nécessaire aux tumeurs pour avoir une croissance soutenue et pour cela ils ont créé un système génétique chez la souris sur lesquelles ils pouvaient contrôler, en temps réel, l'expression d'EGFR qui avait subi une mutation, avec un médicament, la Tétracycline. Ils ont découvert que la croissance des tumeurs s'arrête pendant une période de temps, sous l'effet de la Tétracycline qui bloque EGFR. Mais les tumeurs finissent par reprendre leur progression, même sans EGFR, ce qui signife que quelque chose d'autre provoque cette croissance.
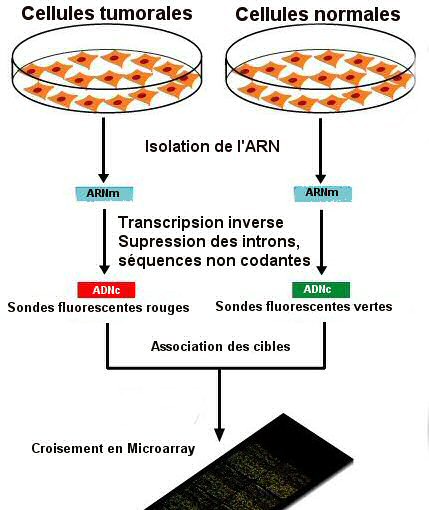
Les chercheurs ont ensuite examiné des tumeurs individuelles qui avaient contourné le besoin de mutation de EGFR pour leur croissance. Dans quelques cas, des tumeurs qui normalement auraient tué des souris en 20 jours étaient toujours stables plusieurs mois après le blocage de EGFR muté. Les scientifiques ont alors utilisé la technologie de microarray pour tester les gènes qui n'étaient pas précédemment exprimés dans les tumeurs et surexprimés dans les tumeurs qui n'exigeaient plus EGFR. Ils ont finalement trouvé le gène, KLHDC8, qui, lorsqu’il est inhibé, bloque la croissance de la tumeur. Cette découverte porte à croire que ce gène pourrait être une cible raisonnable de traitement. Environ la moitié des tumeurs individuelles qui n'ont pas eu besoin d'EGFR muté pour leur croissance ont exprimé ce gène qui lorsqu’il est bloqué provoque l’arrêt de la tumeur. En visant la voie du remplaçant et le récepteur, cela devrait donner une plus longue réponse au traitement parce qu'il frappe l'événement fondamental plus la route d'évasion.
Réf : News Softpedia 20/01/2010
Un nouveau vaccin dendritique sur les cellules souches tumorales, ICT-107.
ImmunoCellular publie le 25/01/2010 les résultats d'un essai clinique dans lequel ils montrent que certains antigènes spécifiques sont très exprimés sur les cellules souches tumorales (CSCs), ce qui suggère que leur vaccin ICT-107 qui vise ces antigènes peut aussi être efficace sur les autres cellules tumorales et éviter les récidives. Les cellules souches CSCs utilisées dans l'étude d'IMUC ont été isolées des tumeurs retirées à la chirurgie de 5 malades avec glioblastome. Ces CSCs ont été trouvées pour avoir de plus hautes expressions de 3 antigènes visé par ICT-107—Her-2/neu, AIM2, et TRP-2—dans les cellules qui composent la tumeur. Les cellules souches tumorales sont comme les racines des mauvaises herbes et les tumeurs récidivent par leurs racines si elles ne sont pas visées efficacement. Dans un essai récent de phase I de ICT-107, les malades avec glioblastome récemment diagnostiqués qui ont reçu le vaccin ont démontré une augmentation à 12 mois dans la survie sans progression (PFS) après chirurgie. Cette survie se compare favorablement avec le PFS médian historique de 6,9 mois observé avec le traitement standard de chirurgie, radiothérapie et chimiothérapie de Temodal. 7/16 malades qui ont participé à l'essai continuent à survivre sans progression de la maladie après plus de 2 ans. Les 6 antigènes tumeur-associés utilisés dans le vaccin ICT-107 sont AIM2, Ses 2/neu, gp-100, MAGE-1, TRP-2 et IL13Ra2. La société pense que ce vaccin est différent de tous les autres et peut être efficace.
Les autres vaccins
Le Dr. Friedman, Duke, n’en démord pas, le vaccin peut être un chimiosensibilisateur et qu’il sera prochainement fiable. Il considère qu’avec le Temodal, Campto-Avastin et les vaccins la guérison est possible. C’est à une avalanche de vaccins que l’on assiste aux Etats-Unis et probablement bientôt en France. Dans son centre, Duke, le Dr Friedman expérimente ERADICATE, un vaccin porté par un virus, le cytomégalovirus. Mais la cible intéressante semble être les antigènes des cellules souches tumorales avec les vaccins dendritiques tel que ICT-107. Les cellules dendritiques sont les sentinelles du système immunitaire pour lui présenter les antigènes, virus ou tumeur. Ces cellules sont les seules capables d’activer les lymphocytes T naïfs et de déclencher une réponse immunitaire. Plusieurs études ont montré, récemment que des cellules dendritiques transfectées avec des ARN messagers d’antigènes des tumeurs du patient (autologue) sont capables d’induire une réponse immunitaire spécifique et efficace et une réponse clinique. Au Duke,
actuellement, essai de vaccin avec des cellules dendritiques transfectées par ARNm de cellules souches tumorales CD133+BTSC, on se bouscule.
Parmi les autres vaccins
WP 1066 qui cible Stat 3
CDX 110 de Pfizer cible EGFRvIII
Beaucoup d’autres vont suivre.
Temodal Générique
Le Temodal générique est-il pour demain, les tribunaux doivent en décider. Shering est une société allemande au départ, créée en 1871 par le Dr. Shering. Une filiale a ensuite été créée aux Etats-Unis. Mais chacune a pris son indépendance, Shering-Plough l’américaine d’un côté aujourd’hui rachetée par Merck et Shering-AG, l’allemande, de l’autre, rachetée par Bayer. Le Temodal est disputé par le laboratoire Teva qui veut en faire un générique car il considère que le brevet est tombé dans le domaine public, ce que conteste Merck qui prétend qu’il est valable jusqu’en 2014. Affaire à suivre.
L'activité de BRAF induit des gliomes chez les souris quand il est combiné avec la perte Ink4a/Arf ou l'activation de Akt
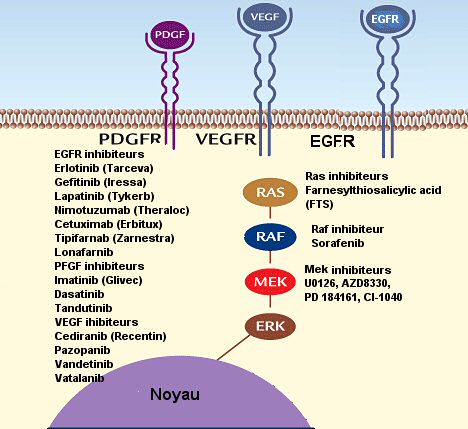
Des mutations dans les récepteurs tyrosine kinase (RTK) du récepteur du facteur de croissance épidermique EGFR, du récepteur du facteur de croissance plaquette dérivé, PDGFR, MET et ERBB2, et une sous activation en aval de RAS/RAF/MEK/ERK, des MAPs kinase, de PI(3)K/Akt, sont trouvées dans presque tout les gliomes de haut grade et la signalisation MAPK (activateur de mitose protéine kinase) est nécessaire pour l'entretien d'une activité soutenue du gliome. De plus, BRAF a subi une mutation dans la majorité des gliomes de bas grade et son expression et son activité est augmentée considérablement dans la majorité de gliomes de haut grade. Bien que l'importance de RTKs et de RAS comme chemin de signalisation clé dans le développement des gliomes ait été déjà démontrée, le rôle de BRAF doit être encore précisé. Les chercheurs ont analysé l'effet de l'activation de BRAF dans la formation des gliomes en utilisant un rétro virus ASLV. Si l'activation de BRAF seul n'est pas suffisante pour une tumorigénèse, la combinaison de BRAF activé et Akt ou BRAF avec la perte Ink4a/Arf assure la formation cancéreuse. Leurs études montrent un rôle pour l'activation de BRAF et sa signalisation dans le développement des gliomes comme une cible potentielle pour la thérapie des gliomes.
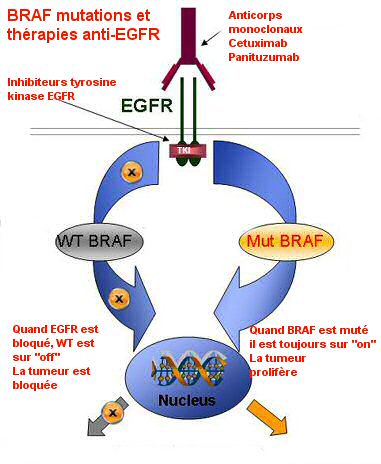
Les mutations d'un gène, BRAF, prédisent la sensibilité à une classe nouvelle de médicaments.
BRAF est une protéine qui joue un rôle central dans la croissance et la survie des cellules cancéreuses. Cette protéine est mutée dans de nombreux cancers et les gliomes. Toutes les tumeurs ayant une mutation BRAF et certaines ayant une mutation RAS sont sensibles aux médicaments qui inhibent MEK. Des essais cliniques sont actuellement en cours. Les FTI, inhibiteurs de farnésyl transférase, en amont de MEK, Ras, Raf, et en aval, Erk, sont Tipifarnib, Zarnestra-R11577), Lonafarnib, Sorafenib. Tous ces médicament bloquent le passage de RAF vers MEK. Tous ces médicaments qui inhibent Mek inhibent aussi sélectivement la croissance des tumeurs cancéreuses qui ont une mutation du gène BRAF. Un de ces médicaments, PD0325901 (Stemolecule), développé par Pfizer, est maintenant testé chez des patients porteurs d'un glioblastome. Ce médicament a toute son efficacité si les autres voies PI3K et NF-Kappa B sont bloquées.
La contestation des thérapies anti-angiogéniques
Plusieurs équipes de chercheurs, tout en reconnaissant une réelle efficacité aux thérapies anti-angiogéniques dans les tumeurs malignes de cerveau, en constatant bien, dès le début du traitement, une action anti-tumorale importante, font part de leurs craintes. Dans les modèles qu’ils ont étudiés sur la souris, ils ont observé de bons résultats mais aussi de façon concomitante, une adaptation de la tumeur vers une plus grande malignité et une plus grande invasion. D’autres voix s’élèvent pour défendre l’efficacité des traitements anti-angiogéniques sur le court terme avec une survie sans progression à 6 mois de l’essai du Dr. Friedman de 28,2% pour Avastin seul et de 37,8% pour Campto-Avastin. Ils admettent que cette amélioration de la PFS 6 mois peut ne pas se traduire par une survie totale améliorée. Comprendre le mécanisme de résistance des tumeurs est le nouveau défi de la neuro-oncologie.
Voici les résultats des essais Avastin ou Campto-Avastin à ce jour.
1-Vredenbourg 2007 35 patients, Campto-Avastin, 57% de répondeurs, 46% de survivants sans progression 6 mois après le début de ce traitement.
2-Chen 2007, 21 patients, 38% de répondeurs, survivants sans progression à 6 mois non communiqués
3-Cloughesy et Friedman 2008/2009 167 patients, Campto seul ou Campto-Avastin, 28,2% de répondeurs avec Avastin seul et 37,8% de répondeurs avec Campto-Avastin, 42,6% de survivants à 6 mois sans progression et 50,3% avec Campto-Avastin
4-Kriesl, 2009, 48 patients, Avastin seul et Campto-Avastin à la récidive, 35% de répondeurs, 29% de survivants sans progression à 6 mois.
Un site utile pour les malades sous corticoïdes
Les patients sous corticoïdes savent qu’ils doivent éviter le sel. Mais comment reconnaître les aliments qui en contiennent beaucoup. Il existe un petit logiciel « Madam », un comparateur, que l’on peut retrouver en saisissant « madam » sur Google, et de cliquer sur le 1er site :
http://www.mangerbouger.fr/madam/
Selon les produits, le sucre, le gras et le sel sont mentionnés.
On choisit sa famille d’aliments, soupe, yaourt, fromages… et on connait immédiatement le poids en sel du produit. Certains résultats surprennent. Consommer des céréales au petit déjeuner pour garder la ligne avec du lait écrémé, apporte 1g de sel pour un besoin quotidien de 6 grammes.
Le 1er essai pour détruire l’incubateur des cellules souches tumorales a commencé
Le produit s’appelle le DepoCyt et il s’agit d’une injection directe du produit encapsulé avec un liposome directement dans le ventricule latéral, en une zone précise avec un cathéter.
L’analyse microarray des
glioblastomes
Sur 30 échantillons de glioblastome analysés au Japon en 2004, par GenoSensor Array 300, on constate :
Amplification
PFC2/CYLN2 (63.3%), cytoplasmique linker 2
EGFR (53.3%),
IL6(53.3%), interleukine
ABCB1 (MDR1) (36.7%), multidrogre-resistant-1
PDGFRA (26.7%). Récepteur du facteur de croissance plaquettes-dérivé
Suppression
FGFR2(66.7%), facteur de croissance du fibroblaste
MTAP (60.0%), méthylthioadénosine phosphorylase
DMBT1 (56.7%), sur 10q, gène suppresseur de tumeur
CDKN2A (p16)/MTAP (50.0%), cycline dependant kinase
PIK3CA (43.3%), Phosphatidylinositol 3-kinase
EGR2 (43.3%), Early Growth reponse 2
Rarement suppression de RB1 ouTP53
Les pertes les plus fréquentes sont sur les chromosomes 7, 10 et 14, avec la suppression des bras longs 7q (33,3%), 10q (46,7%) et 17q (13,3%), du bras court 7p (20%). On observe la perte totale du chromosome 10 dans 13/30 cas (30%), souvent accompagnée d’une amplification d’EGFR (7/13 cas, 77,8%).
Les analyses génétiques seront demain de routine pour les thérapies.
Les derniers essais cliniques en cours
d’après les sites Clinicaltrials, Orphanet, EORTC
1-(01/10), E.-U., Sloan Kettering, I/II, Perifosine+Temsirolimus pour glioblastome en récidive. Perifosine est un inhibiteur oral d’AKT et de RAS/ERK qui vise les cellules progénitrices gliales.
2-(12/09) Belgique, Radiochimiothérapie standard de Temodal + Cilengitide (IV 2000mg 2 fois par semaine) ou Cetuximab (IV 250 mg/m2, 1 fois par semaine. Pour patients avec glioblastome nouvellement diagnostiqué. MGMT actif, non méthylé. (III)
3-(01/10), E.-U., DM-CHOC-PEN (Penclomedine), IV toutes les 3 semaines pour glioblastome nouvellement diagnostiqué (I). Penclomedine avait montré des effets antinéoplasiques intéressants en préclinique pour les tumeurs avec mutation du gène P53. Ici on ne regarde pas.
4-(01/10), E.U ., I/II, DepoCyt , Ara-C ou Cytarabine liposomiale en intraventriculaire pour viser les cellules progénitrices des cellules souches tumorales dans leur incubateur, le ventricule latéral. Pour glioblastome récurrent en complément du Temodal 75 mg/m2 21/28 jours. L’injection, toutes les 2 à 4 semaines devra être confiée à des neurochirurgiens spécialistes de ces chimios par cathéter.
5-France (01/10), I/II, CLCC François Leclerc, modulation de la radiothérapie pour glioblastome nouvellement diagnostiqué. Des doses variables de radiothérapie de 52 à 80 grays en 28, 30 ou 32 jours. Le bilan sera rapidement fait 3 mois après.
6-France (01/10), III, CLCC Leclerc, Anocef, Campto-Avastin néoadjuvant et adjuvant + radiochimiothérapie de Temodal versus radiochimiothérapie de Temodal pour glioblastome inopérable.
7-E.-U. (09/09) E.-U., II, GDC-O449, inhibiteur oral de Sonic Hedgehog, chaque jour pendant 7 jours avant la chirurgie pour patients avec glioblastome pouvant être réopéré à la récidive
8-(10/2009), E.-U.,II, Robert H. Lurie, Bortezomib en IV jours 1, 4, 8, puis toutes les 2 semaines après chirurgie +Temodal pour gliome malin en récidive pouvant être réopérés. Bortezomib est un inhibiteur de la voie NF-Kappa B.
9-(09/09), E.-U., I, Glivec+Cilengitide pour glioblastome en récidive.
10-R.-U., I, BIB2992 +Temodal (si MGMT silencieux) + radiothérapie pour glioblastome nouvellement diagnostiqué. BIB 2992 est un inhibiteur d’EGFR. Semaine mondiale et marche mondiale contre les tumeurs cérébrales organisée par IBTA
La semaine mondiale de sensibilisation aux tumeurs cérébrales a eu lieu du 1er au 7 novembre 2009. 3 marches ont été organisées pour la France.
1-Marie pour la 3ème fois a organisé une marche à La Palmyre-La Tremblade (17) le samedi 11/10/2009 le long de l’Océan Atlantique, 54 marcheurs ont fait chacun 6 kilomètres et 30 cyclistes ont fait 15 kilomètres en VTT. Les 84 participants avaient entre 3 et 80 ans. 831,80 euros ont été récoltés et reversés à l’ARTC. 774 kms ajoutés à la
marche mondiale. La marche s’est terminée par un joyeux pique nique sur la plage.
2-Bernard, le mari d’Agnès a organisé pour la 1ère fois, une marche au départ de l’Opéra Bastille à Paris, le samedi 1er novembre 2009, 8 kms sous la pluie pour les 26 participants, le long d’une ancienne voie de chemin de fer, boisée aujourd’hui jusqu’à Porte Dorée. Les participants ont reçu un beau tee-shirt
3-Pour la 2ème fois, GFME a organisé une marche le samedi 7 novembre dans l’un des plus beaux parcs de Marseille à côté des plages du Prado, le Parc Borely. Les 15 participants venus de Paris, de Lyon, de la Loire ont bravé la pluie battante pour réaliser à pied les 1,4 kms du parcours. 1350 euros recueillis par une participante lors du décès de son mari ont été adressés à l’ARTC.
A tous les participants et donateurs, bravo et merci. Avec 1003 kms et 125 participants, la France se classe honorablement au niveau mondial sur les 226.000 kms parcourus avec 38.000 participants. Nous ferons d’autres marches en 2010 et nous l’espérons, avec un meilleur temps.
Ils nous ont quittés
Ils ont encore été très nombreux à nous avoir quittés depuis septembre 2009.
-Le 10/09/2009, Valérie, 30 ans, la fille d’Angélo.
-Le 11/09/2009, Philippe, 54 ans, le mari de Jocelyne.
-Le 21/09/2009, Michèle, 62 ans, la maman de Céline.
-Le 26/09/09, Claudette, 64 ans, la maman de Josée.
-Le 30/09/2009, Nicole, 64 ans, l’épouse de Maurice.
-Le 30/09/2009, Stéphane, 36 ans, le beau frère de Nadège.
-Le 30/09/2009, Jean-Louis, 67 ans, le papa de Carole.
-Le 11/10/2009, Claude, le frère de Françoise.
-Le 20/10/2009, Jacques, 46 ans, le mari de Sylvie, le papa de Camille
-Le 26/10/2009, Kadi, 67 ans, le papa de Ahlem
-Le 30/10/2009, Fernando, 60 ans, le mari de Zaza
-Le 03/11/2009, Jeannine, 65 ans, la maman de Pascale
-Le 06/11/2009, Georgette, 70 ans, la maman d’Emmanuelle
-Le 13/11/2009, Alexandre, 59 ans, le mari de Rimma, le papa de Macha et Micha
-Le 17/11/2009, Anne, 29 ans, la fille d’Anne
-Le 26/11/2009, Guy, 63 ans, le beau père de Paolo.
-Le 18/12/2009, James, 4 ans, le neveu de Marie Tête.
-Le 28/12/2009, Hubert, 67 ans, le papa d’Agnès.
-Le 13/01/2010, le papa de Catherine, 64 ans.
-Le 19/01/2010, Jérome, 44 ans, le mari de la nièce de Michel en Espagne.
-Le 19/01/2010, Ginette, 75 ans, la belle mère de François.
-Le 23/01/2010, Pierre-François, 50 ans, le mari d’Anne-Claude,
-Le 20/01/2010, Margot, 7 ans, la fille d’Elodie et Emmanuel, la nièce de Nathalie
A toutes les familles, GFME adresse ses plus sincères condoléances.
Mailing-listes, des adhérents toujours plus nombreux
Les mailing listes de GFME totalisent aujourd’hui 547 adhérents, ce qui se compare favorablement à la liste américaine Brain-Temozolomide qui en totalise 2164. 346 sur la liste gfme et 201 sur la liste astrocytome GFME. 9 mails en moyenne journalière de janvier 2010 pour la liste GFME et 0,8 message pour la liste astrocytome-gfme.
Le site Internet, en forte croissance
3 hébergeurs pour le site
http://gfme.free.fr/
http://membres.lycos.fr/gfme/
http://asso.orpha.net/GFME/index.html
La fréquentation du site est en forte croissance en fin d’année 2009 et début 2010 avec un dépassement de 1200 visites journalières en janvier. Le record a été battu le 5 octobre avec 1698 visites. Comparés aux mêmes mois de 2008, il y avait 34968 visiteurs en 10/09, 35355 en 11/09, 33641 en 12/09 et 37324 en 01/10 soit 141288 visiteurs contre 27816 visiteurs en 10/08, 27660 en 11/08, 25398 en 12/08, 29806 en 8/08 soit un total de 110680 visiteurs, une augmentation de 27,6%. La moyenne mensuelle pour les 4 derniers mois écoulés de 2009/2010 s’établit à 1148 visites par jour contre 899 visites journalières sur la même période de 2008/2009. Sur l’origine des visiteurs, France 71%, Etats-Unis 6%, Canada 4%, Belgique 3%, Suisse 2%, Tunisie 1%, Algérie 1%, Russie 1%, Maroc 0,5%, Allemagne 0,6%, Chine 0,3%, Luxembourg 0,3%, Grèce 0,3%, Italie 0,2%, Espagne 0,2%. Parmi les motes saisis dans le moteur de recherche, tumeur au cerveau, symptômes, glioblastome, cortisone. Maximum de fréquentation 17h avec une fréquentation sur 24h et une crête entre 10h et 22h.

***************************
Rendez-vous pour le prochain numéro, le n° 17 en Février 2010.
Glioblastome Association
Michèle Esnault (GFME)
Bât A, boîte 4
22 Bd Camille Flammarion
13001 Marseille.
Téléphone 04.91.64.55.86 ou 06.82.73.11.84
Adhésion 15 euros.
Renouvellement 7,5 euros.
Reçu fiscal pour déduction d’impôt.
CCP Marseille 15.349.73N