23/05/2022
GFME, connaissances
Suite

Cliquer pour agrandir
La radiorésistance par action sur p53
Les cellules de glioblastome produisent des cytokines aux caractéristiques pro-inflammatoires ou immunosuppressives, ou les deux, et qui, sans compter qu'elles modifient l'expression du gène p53, sont associées à la résistance du glioblastome à la radiothérapie. Les données sur les cytokines qui ont fait l'objet de rapports sont isolées et parfois divergentes et une analyse détaillée du profil des cytokines et de leur récepteurs correspondants dans des glioblastomes irradiés a attiré peu d'attention. La présente étude visait à vérifier l'hypothèse selon laquelle la radiothérapie administrée à des doses pertinentes sur le plan clinique ne modifierait pas de façon significative, à elle seule, l'expression des cytokines endogènes et de leurs récepteurs dans les lignées de cellules de glioblastome humain comportant un gène p53 du type sauvage et mutant. Conception et méthode : On a irradié avec du cobalt 60 à une dose de 10 Gy des spécimens de culture de quatre lignées de cellules de glioblastome présentant une expression différente du gène p53 (U87, U118, U251, U373). Après 48 heures, on a défini la radiosensibilité au moyen d'une épreuve de formation de cellules souches, analysé la répartition du cycle cellulaire par cytométrie de flux et défini au moyen d'une épreuve de protection de la RNase les profils de l'ARN messager (ARNm) des cytokines et de leurs récepteurs. On a appliqué à des lignées de cellules p53 du type sauvage des doses uniques différentes de rayonnement à intervalles différents après les cultures.
Résultats
Toutes les lignées de cellules étaient relativement radiorésistantes à des doses plus faibles de 1 et 2 Grays.
p53 le gène suppresseur de tumeur
Le gène p53 est situé sur le bras court du chromosome 17 en position p13.1 Le gène a été très conservé pendant l'évolution . La protéine p53 est une phosphoprotéine de 393 acides aminés de poids moléculaire 53 kDa. On la trouve en très petite quantité dans les cellules normales, mais en grande abondance dans les cellulestumorales.
Action de la protéine p53
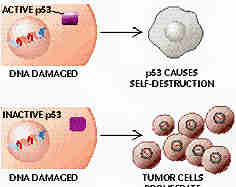
La fonction première de la protéine p53 est d’agir en tant que facteur de transcription. Elle fonctionne en se fixant de manière spécifique sur les régions régulatrices de gènes dont elle contrôle l’expression. Dans une cellule normale, en l’absence de tout stress, il n’y a que très peu de p53, car celle-ci n’est pas nécessaire au fonctionnement de la cellule. Cette absence de p53 est due à l'enzyme mdm2 qui, en se fixant sur p53, induit sa destruction. Lorsque la cellule se trouve en situation de stress, l’association entre p53 et mdm2 est abolie ce qui conduit à une augmentation de la quantité de p53 dans la cellule. Cette première phase est nommée « phase d’activation ». De nombreux types de stress sont capables d’activer la p53 comme les lésions de l’ADN, les défauts de division ou de métabolisme cellulaire. Dans un second temps, la p53 va subir de nombreuses modifications post traductionnelles qui vont permettre d’activer sa fonction de facteur de transcription. Cette phase est nommée « phase de modification ». Dans un troisième temps, la p53 activera la transcription d’un grand nombre de gènes. Cette phase est nommée « phase de réponse ». L’ensemble de ce programme pourra conduire à deux résultats, soit l’arrêt du cycle cellulaire soit l’apoptose. L’arrêt du cycle cellulaire permet à la cellule de stimuler ses mécanismes de réparation, dont certains sont directement activés par p53. Lorsque la réparation est effectuée, le taux de p53 retourne à la normale et le cycle cellulaire reprend. Si les dommages subis par la cellule ne peuvent pas être réparés, la cellule entre en apoptose, ce qui conduit à son élimination.
Deux rôles pour cette protéine : soit l'arrêt du cycle cellulaire entre la phase G 1 et la phase S, soit la mort cellulaire par apoptose. La protéine p53 se lie avec une séquence spécifique d'ADN (c'est donc un facteur de transcription) aboutissant à une interaction avec le cycle cellulaire par l'intermédiaire d'un gène appelé WAF1 / Cip1, (pour Wild Type p53-activated fragment et cdk2 inhibiting protein) dont la protéine p21 se lie aux kinases cdk2, et inhibe leur activité. La cellule s'arrête avant la synthèse de l'ADN et peut réparer d'éventuels dommages. De nombreux stimuli provoquent l'augmentation de la p53, notamment l'irradiation par les rayons X ou gamma. Dans d'autres cellules, l'augmentation de la protéine p53 induite par l'irradiation provoque l'induction de l'apoptose ou mort programmée, que l'on peut interpréter comme la solution préférentielle pour l'organisme quand la réparation de l'ADN n'est pas possible.
p53 et les glioblastomes
Les fibroblastes de malades atteints de certains cancers (syndrome de Li-Fraumeni) ne contiennent qu' un seul allèle du gène p53 et leurs cellules ne sont pas tumorigènes. Après de nombreuses divisions, quelques cellules vont perdre l'allèle restant p53 et devenir rapidement angiogéniques et tumorigènes , et ne fabriquent plus de thrombospondine . Le gène p53 pourrait agir aussi sur la synthèse de l'interféron a (a -IFN).
Dans certaines lignées cellulaires de glioblastomes, il existe une délétion du gène p53. Si on les fait réexprimer le gène, on observe une disparition du pouvoir angiogénique, avec réapparition de la synthèse de a-IFN . La disparition de la synthèse des inhibiteurs de l'angiogenèse (par exemple la thrombospondine , dont le gène est proche de certains gènes suppresseurs et notamment le p53, expliquerait la vascularisation accrue des tumeurs. Les cellules de la tumeur dormante peuvent perdre des gènes suppresseurs de tumeur, ou inhibiteurs d'angiogenèse et se mettre à sécréter des facteurs angiogéniques, la tumeur ainsi bien oxygénée peut se développer de façon rapide. Les traitements seront différents selon la présence ou non d'une modification génétique comme la délétion de P53 par exemple.
RITA restitue les fonctions de p53 dans les cellules tumorales.
Impliquée dans la plupart des tumeurs malignes, la dérégulation de p53 compromet l'apoptose habituellement programmée par toute altération du génome. Les mutations du gène p53 concernent environ 50% des cancers et, dans les tumeurs où le gène n'est pas muté, il existe fréquemment une altération fonctionnelle de la protéine. Cette altération est fréquemment le fait d'une dégradation anormale de p53 par le protéasome. Cette dégradation est favorisée par la fixation de p53 à HDM-2 ( Human Double Minute-2 ). Cette protéine se fixe au p53 au niveau de sa région amino-terminale, inhibe ses fonctions transactivatrices et la cible pour la dégradation par le protéasome. Dans la Revue de presse 136 du 11 juin 2002, Rafaël Levy nous reportait le travail de Bykov et al. où un composé chimique avait la capacité de restaurer les capacités de liaison de p53 à l'ADN ainsi que ses capacités de transactivation, dans des cellules où p53 était muté. Plus récemment, un groupe suédois a criblé des lignées cellulaires avec la banque de produits chimiques du NCI ( National Cancer Institute ). Un composé, RITA, avait la capacité d'inhiber la croissance de cellules de cancer du côlon avec p53 fonctionnelle alors que le même produit avait un effet négligeable sur des cellules n'exprimant pas p53. RITA doit son nom à sa propriété de réactivation de p53 : Reactivation of p53 and Induction of Tumor Cell Apoptosis . La fixation de RITA à p53 in vitro induit une accumulation de cellules. RITA bloque l'interaction p53-HDM-2, réactive ses fonctions transactivatrices et induit l'apoptose médiée par la protéine suppresseur de tumeurs. In vivo enfin, RITA possède un effet antitumoral sur les tumeurs greffées à la souris SCID.
Clairement, RITA constitue une nouvelle arme thérapeutique potentielle à développer.