GFME, connaissances
Suite

Cliquer pour agrandir
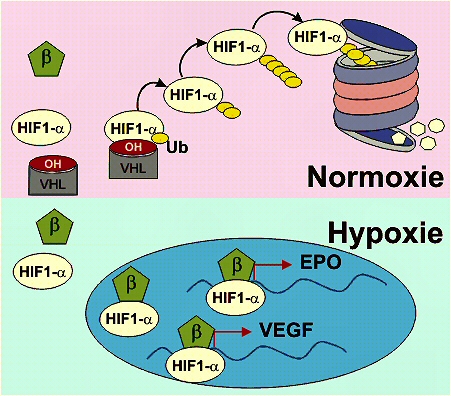
HIF-1 alpha Le facteur induit par l'hypoxie (HIF-1 alpha)
Le facteurs induit par l’hypoxie (ou HIF, de l’anglais Hypoxia Inducible Factor) est une protéine qui agit comme un facteur de transcription et qui est induit par l’absence d’oxygène. D’un point de vue physiologique, l’hypoxie provoque la sécrétion d'érythropoïétine (EPO) qui stimule la production de globules rouges, pour améliorer le transport d’oxygène aux tissus. Cette signalisation est assurée par HIF-1 alpha, le plus actif de la famille des HIFs. Cette protéine a été découverte en 1992 Gregg Semanza qui étudiait l'EPO. En fait, c'est une séquence située en position 3’ non-codante dans le promoteur de l’EPO, qui porte le nom d’élément réponse à l'hypoxie, hypoxia response element (HRE) et qui fixe la protéine HIF-1 en situation d’hypoxie. Par la suite, la séquence HRE a aussi été localisée sur plus de 70 autres gènes, tels le facteur de croissance vasculaire, vascular endothelial growth factor (VEGF). HIF-1 alpha comprend 826 acides aminés. On la retrouve constituée de 15 exons, sur le chromosome 14 (14q21-q24). HIF-1 bêta contient 789 acides aminés et est située sur le chromosome 1 (1q21), et aussi appelé ARNT1, pour aryl hydrocarbon receptor nuclear translocator et est exprimée dans le noyau de la cellule pour la détoxification de celle-ci. Par contre, on retrouve HIF-1 alpha, uniquement en situation d’hypoxie. HIF-1 alpha ne possède une demie-vie que de seulement 5 minutes dans le cytoplasme. Lors d’un retour aux conditions normales d’oxygène, les protéines HIF-1 alpha se trouvant dans le noyau seront dégradées par le protéasome nucléaire. Bien que l’hypoxie soit le principal activateur de HIF-1 alpha, ce n’est pas toujours l’EPO qui est synthétisé, mais bien d’autres protéines comme le VEGF qui augmente l’angiogénèse, aussi lors du développement embryonnaire ou dans les cancers.
L'inhibition de la vascularisation, mais pas l'angiogenèse, empêche les récidives du glioblastome après irradiation chez la souris
GFME 24/02/2010 n° 297
Retrouver l'article original
J Clin Invest. 22 février 2010
Auteurs :
Kioi M, Vogel H, Schultz G, Hoffman RM, Harsh GR, Brown JM.
Malgré les fortes doses d'irradiation délivrées dans le traitement des patients atteints de glioblastome, les tumeurs récidivent inévitablement à l'intérieur du champ d'irradiation, ce qui entraîne un taux de guérison faible. Comprendre le mécanisme de la récidive est donc important. Ici, nous avons montré dans un modèle de xénogreffe de glioblastome intracrânienne que l'irradiation induit le recrutement depuis la moelle osseuse, de cellules dendritiques dérivées(BMDCs) dans les tumeurs, le rétablissement de la radio-vascularité endommagée par vasculogenèse, permettant ainsi la croissance des cellules cancéreuses et leur survie. L'afflux de ces cellules dendritiques BMDCs est initié par l'induction de HIF-1 dans les tumeurs irradiées, et le blocage de cet afflux a empêché les récidives tumorales. Des études antérieures ont démontré que les BMDCs sont recrutées par les tumeurs en partie grâce à l'interaction entre HIF-1, SDF-1 (Stromal-derived factor 1) et son récepteur, CXCR4. L'inhibition pharmacologique de HIF-1 ou de l'interaction SDF-1/CXCR4 a empêché l'afflux des BMDCs, principalement CD11b et myélomonocytes, radio-induits et le développement de la vascularisation tumorale fonctionnelle, ce qui a entraîné l'abrogation de la récidive tumorale. Des résultats similaires ont été obtenus en utilisant des anticorps neutralisants le récepteur CXCR4. Nos données suggèrent donc une nouvelle approche pour le traitement du glioblastome, en plus de la radiothérapie, le blocage de la voie de la vasculogenèse qui peut être accompli en utilisant le médicament AMD3100, qui est déjà cliniquement approuvé, petite molécule inhibant les intéractions SDF-1/CXCR4.
Un peu de vocabulaire :
BMDCs : Bone Marrow dérived Dentritic Cell, cellule dendritique dérivée de la moelle osseuse
SDF-1 : (stromal-derived factor-1), chimiokine jouant un rôle majeur au cours de l'embryogenèse. SDF-1 et son unique récepteur CXCR4 sont impliqués dans la différenciation des cellules progénitrices.
HIF-1: Facteur inductible par hypoxie 1, protéine composée par 2 subunités : HIF-1a et HIF-1b. Dans une situation de manque d'oxygène comme c'est le cas de l'hypoxie, HIF-1a ne se dégrade pas, mais s'unit à HIF-1b pour donner HIF-1 et provoquer l'activation et à la stimulation de différents gènes.
Pubmed : 20179352